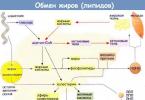
Lipidele resintetizate în intestin sunt transportate ca parte a chilomicronilor cu limfa.Lipidele sunt insolubile în apă, deci sunt transportate în asociere cu proteine.
Lipoproteinele sunt complexe de proteine și lipide, forma de transport al lipidelor în sânge. Lipide LP: trigliceride, fosfolipide, colesterol. Proteinele LP sunt apoproteine ale unor clase individuale de LP.
Funcțiile apoproteinelor sunt structurale (LP), de transport, secretoare (necesare pentru secreția de LP de către celulele hepatice și intestinale), necesare interacțiunii LP cu receptorii, activează enzimele implicate în metabolismul LP, conferă lipidelor solubilitate în apă. , apoproteina A1 din HDL activează LCAT.
Structura lipoproteinelor. Miezul hidrofob (esteri de colesterol, TG) este înconjurat la exterior de fosfolipide, colesterol liber și apoproteine.
Clasificarea medicamentelor.
pe baza mobilității în câmpul electric: - ChMs rămân la început, - alții migrează în zonele globulinice: ß-LP, pre-ß-LP, α-LP.
În funcție de densitatea hidratată (folosind metoda ultracentrifugării), medicamentele sunt împărțite în CM, VLDL, LDPP, LDL și HDL.
Rolul biologic al medicamentelor. TG endogene sunt livrate celulelor periferice pentru a satisface nevoile de energie, iar colesterolul endogen este livrat la biosinteza membranei.
Compoziția și proprietățile lipoproteinelor.
Chilomicronii transportă TG exogen, colesterol, fosfolipide și grăsimi alimentare din intestin către țesuturi prin sistemul limfatic. CM imature sunt sintetizate în enterocite, care intră mai întâi în limfă și apoi în sânge. Apoproteina principală a CM, proteina B-48, este sintetizată în celulele mucoasei intestinale și este necesară pentru formarea structurii CM. În sânge, CM imature primesc alte apoproteine din HDL - C- și E- și sunt transformate în CM mature. Primul organ prin care trebuie să treacă chimioterapia sunt plămânii. Când CM intră în fluxul sanguin din intestin, mastocitele sunt activate cu eliberarea de heparină și activarea lipoprotein lipazei.
Lipemia adsorbtivă este o creștere a cantității de lipide din sânge care apare după masă.
Lipoprotein lipaza (factorul de clearing) hidrolizează TAG în CM și VLDL, este localizată în endoteliul capilarelor diferitelor organe, este activată de heparină și o creștere a TAG în sânge. Chilomicronii TAG sunt clivați la suprafața și în interiorul hepatocitelor, pe suprafața endoteliului capilarelor de țesut adipos.
VLDL și HDL sunt secretate în sânge de ficat, unde sunt sintetizate. LDL se formează în fluxul sanguin din VLDL ca rezultat al hidrolizei porțiunii TG a VLDL de către lipoprotein lipaza.
Soarta LDL. Există receptori pentru LDL pe membranele plasmatice ale celulelor. LDL pătrunde în celule, unde, sub influența hidrolazelor lizozomale, se descompun în componentele lor constitutive, colesterolul liber este inclus în membrana plasmatică sau este esterificat și depus sub formă de esteri în citoplasmă. Este posibilă endocitoza nespecifică a LDL.
HDL transportă colesterolul la ficat. În ficat, colesterolul este oxidat în acizi biliari și eliminat prin intestine. Oxidarea colesterolului are loc în ficat de către sistemul monooxigenazei. Colesterolul 7a-hidroxilaza este o enzimă care limitează viteza. HDL este capabil să accepte colesterolul din membranele celulare.
Conversia colesterolului liber în esterificat: colesterol + lecitină → lisolecitină + ester de colesterol. Esterul colesterolului se formează pe suprafața HDL și se transferă în miezul HDL.
O scădere a colesterolului HDL în plasma sanguină este asociată cu o scădere a LCAT, a numărului de particule HDL, lecitină și apoproteina A1.
Jumătate de viață. HM – mai puțin de o oră, VLDL – 2-4 ore, LDL – 2-4 zile, HDL – 5 zile. LDL și HDL sunt absorbite prin endocitoză de către celulele ficatului, intestinelor, țesutului adipos, rinichilor și glandelor suprarenale și sunt distruse în lizozomi.
Acizi grași neesterificați (NEFA). Acizii grași din plasma sanguină sunt sub formă esterificată: în compoziția fosfolipidelor, esterilor de colesterol, mono-, di-, trigliceridelor. În formă liberă, acizii grași sunt transportați în plasmă din țesutul adipos și ficat către mușchii scheletici, caz în care se leagă de albumină.
NEFA intră în plasma sanguină ca urmare a lipolizei TG, catalizată de lipază în țesutul adipos; se formează prin acțiunea lipoprotein-lipazei asupra TG a plasmei sanguine în timpul tranziției lor în țesuturi; acizi grași cu o lungime a lanțului mai mică de 1o atomi de carbon sunt absorbiți în formă neesterificată prin sistemul circulator portal și intră în ficat (acest lucru este important pentru copii, deoarece laptele este bogat în acizi grași cu lanț scurt).
Triacilgliceridele sunt o formă de transport pentru acizii grași saturați. Fosfolipidele și colesterolul sunt o formă de transport pentru acizii grași polinesaturați.
Funcțiile NEFA - furnizează 50% din energie în timpul postului, material energetic pentru miocard, mușchi, rinichi, ficat, acizii grași saturați îndeplinesc energie, iar acizii grași nesaturați îndeplinesc funcții plastice.
Răspuns. Amoniacul, glutamina și ionul de amoniu NH 4 + cresc în sângele pacientului.
Transportul lipidelor în organism are loc în două moduri:
- 1) acizii grași sunt transportați în sânge cu ajutorul albuminelor;
- 2) TG, FL, HS, EHS etc. Lipidele sunt transportate în sânge ca parte a lipoproteinelor.
Metabolismul lipoproteinelor
Lipoproteinele (LP) sunt complexe supramoleculare sferice formate din lipide, proteine și carbohidrați. LP-urile au o înveliș hidrofilă și un miez hidrofob. Învelișul hidrofil include proteine și lipide amfifile - PL, colesterol. Miezul hidrofob include lipide hidrofobe - TG, esteri de colesterol etc. LP-urile sunt foarte solubile în apă.
Mai multe tipuri de lipide sunt sintetizate în organism; ele diferă în compoziția chimică, se formează în locuri diferite și transportă lipidele în direcții diferite.
Medicamentele sunt separate folosind:
- 1) electroforeza, dupa sarcina si marime, pe b-LP, v-LP, pre-c-LP si CM;
- 2) centrifugare, după densitate, pentru HDL, LDL, LDLP, VLDL și CM.
Raportul și cantitatea de LP din sânge depind de momentul zilei și de nutriție. În perioada postabsorbtivă și în timpul postului, în sânge sunt prezente doar LDL și HDL.
Principalele tipuri de lipoproteine
Compoziție, % VLDL CM
- (pre-in-LP) DILI
- (pre-în-LP) LDL
- (v-LP) HDL
- (b-LP)
Proteine 2 10 11 22 50
FL 3 18 23 21 27
EHS 3 10 30 42 16
TG 85 55 26 7 3
Densitate, g/ml 0,92-0,98 0,96-1,00 0,96-1,00 1,00-1,06 1,06-1,21
Diametru, nm >120 30-100 30-100 21-100 7-15
Funcții Transportul lipidelor alimentare exogene către țesuturi Transportul lipidelor endogene ale ficatului către țesuturi Transportul lipidelor endogene ale ficatului către țesuturi Transportul colesterolului
în țesut Îndepărtarea excesului de colesterol
din tesaturi
apo A, C, E
Locul de formare a enterocitelor hepatocitului în sânge din VLDL în sânge din hepatocitul LDLP
Apo B-48, C-II, E B-100, C-II, E B-100, E B-100 A-I C-II, E, D
Normal în sânge< 2,2 ммоль/л 0,9- 1,9 ммоль/л
Apobelki
Proteinele care compun medicamentul se numesc apoproteine (apoproteine, apo). Cele mai comune apoproteine includ: apo A-I, A-II, B-48, B-100, C-I, C-II, C-III, D, E. Apoproteinele pot fi periferice (hidrofile: A-II, C-II, E) și integrală (au o regiune hidrofobă: B-48, B-100). Transferul apos periferic între LP, dar apos integral nu. Apoproteinele îndeplinesc mai multe funcții:
Funcţia apoproteică Locul de formare Localizare
A-I Activator LCAT, formarea ECS hepatic HDL
Activator A-II al LCAT, formarea ECS HDL, CM
B-48 Enterocitul XM structural (sinteză LP), receptor (fagocitoză LP)
B-100 structural (sinteză LP), receptor (fagocitoză LP) ficat VLDL, LDPP, LDL
Activator C-I LCAT, formarea ECS Liver HDL, VLDL
Activator C-II LPL, stimulează hidroliza TG în lipoproteina Ficat HDL > CM, VLDL
Inhibitor C-III LPL, inhibă hidroliza TG în ficatul LP HDL > CM, VLDL
D Transfer ester colesteril (CET) HDL hepatic
E Receptor, fagocitoză LP ficat HDL > CM, VLDL, LDLP
Enzime de transport al lipidelor
Lipoprotein lipaza (LPL) (EC 3.1.1.34, gena LPL, aproximativ 40 de alele defecte) este asociată cu sulfatul de heparan situat pe suprafața celulelor endoteliale ale capilarelor vaselor de sânge. Hidrolizează TG din compoziția medicamentului la glicerol și 3 acizi grași. Odată cu pierderea TG, CM se transformă în CM rezidual, iar VLDL își crește densitatea la LDLP și LDL.
Apo C-II LP activează LPL, iar fosfolipidele LP sunt implicate în legarea LPL la suprafața LP. Sinteza LPL este indusă de insulină. Apo C-III inhibă LPL.
LPL este sintetizat în celulele multor țesuturi: grăsime, mușchi, plămâni, splină, celule ale glandei mamare care alăptează. Nu este în ficat. Izoenzimele LPL ale diferitelor țesuturi diferă în valorile Km. În țesutul adipos, LPL are Km de 10 ori mai mare decât în miocard, prin urmare, țesutul adipos absoarbe acizii grași doar atunci când există un exces de TG în sânge, iar miocardul în mod constant, chiar și cu o concentrație scăzută de TG în sânge. Acizii grași din adipocite sunt utilizați pentru sinteza TG, în miocard ca sursă de energie.
Lipaza hepatică este localizată pe suprafața hepatocitelor; nu acționează asupra colesterolului matur, ci hidrolizează TG în LDPP.
Lecitină: colesterol acil transferaza (LCAT) este localizată în HDL, transferă acil din lecitină în colesterol pentru a forma ECL și lisolecitină. Este activat de apo A-I, A-II și C-I.
lecitină + CS > lisolecitină + ECS
ECS este scufundat în nucleul HDL sau transferat cu participarea apo D către alte HDL.
Receptorii de transport lipidic
Receptorul LDL este o proteină complexă constând din 5 domenii și care conține o parte de carbohidrați. Receptorul LDL interacționează cu proteinele ano B-100 și apo E, leagă bine LDL, mai rău decât DILI, VLDL și CM rezidual care conține aceste apos. Celulele tisulare conțin un număr mare de receptori LDL pe suprafața lor. De exemplu, o celulă fibroblastă are de la 20.000 la 50.000 de receptori.
Dacă cantitatea de colesterol care intră într-o celulă depășește nevoia acesteia, atunci sinteza receptorilor LDL este suprimată, ceea ce reduce fluxul de colesterol din sânge în celule. Când concentrația de colesterol liber în celulă scade, dimpotrivă, sinteza HMG-CoA reductazei și a receptorilor LDL este activată. Hormonii stimulează sinteza receptorilor LDL: insulina și triiodotironina (T3), hormonii sexuali și glucocorticoizii o reduc.
Proteine asemănătoare receptorului LDL Pe suprafața celulelor din multe organe (ficat, creier, placentă), există un alt tip de receptor numit „proteină asemănătoare receptorului LDL”. Acest receptor interacționează cu apo E și captează restul (rezidual) CM și DILI. Deoarece particulele rămase conțin colesterol, acest tip de receptor asigură și intrarea acestuia în țesuturi.
Pe lângă intrarea colesterolului în țesuturi prin endocitoza lipoproteinelor, o anumită cantitate de colesterol pătrunde în celule prin difuzie din LDL și alte lipoproteine la contactul lor cu membranele celulare.
Concentrația normală în sânge este:
- * LDL
- * lipide totale 4-8g/l,
- * TG 0,5-2,1 mmol/l,
- * Acizi grași liberi 400-800 µmol/l
Lipidele sunt insolubile în mediu apos, prin urmare, pentru transportul lor în organism, se formează complexe de lipide cu proteine - lipoproteine (LP). Există transport de lipide exo- și endogen. Exogen include transportul lipidelor primite din alimente, iar endogen include mișcarea lipidelor sintetizate în organism.
Există mai multe tipuri de LP, dar toate au o structură similară - un miez hidrofob și un strat hidrofil la suprafață. Stratul hidrofil este format din proteine numite apoproteine și molecule de lipide amfifile - fosfolipide și colesterol. Grupările hidrofile ale acestor molecule se confruntă cu faza apoasă, iar grupările hidrofobe se confruntă cu miezul, în care se află lipidele transportate. Apoproteinele îndeplinesc mai multe funcții:
· formează structura lipoproteinelor (de exemplu, B-48 este proteina principală a XM, B-100 este proteina principală a VLDL, LDPP, LDL);
· interacționează cu receptorii de pe suprafața celulelor, determinând ce țesuturi vor capta acest tip de lipoproteine (apoproteina B-100, E);
· sunt enzime sau activatori ai enzimelor care acționează asupra lipoproteinelor (C-II - activator al lipoprotein lipazei, A-I - activator al lecitinei: colesterol aciltransferaza).
În timpul transportului exogen, TAG resintetizați în enterocite împreună cu fosfolipidele, colesterolul și proteinele formează CM, iar în această formă sunt secretate mai întâi în limfă și apoi în sânge. În limfă și sânge, apoproteinele E (apo E) și C-II (apo C-II) sunt transferate de la HDL la CM, transformând astfel CM în unele „mature”. ChM-urile sunt destul de mari ca dimensiuni, așa că, după ce consumă o masă grasă, dau plasmei sanguine un aspect opalescent, asemănător laptelui. Odată ajunse în sistemul circulator, CM suferă rapid catabolism și dispar în câteva ore. Timpul de distrugere a CM depinde de hidroliza TAG sub acțiunea lipoprotein lipazei (LPL). Această enzimă este sintetizată și secretată de țesuturile adipoase și musculare și de celulele glandei mamare. LPL secretat se leagă de suprafața celulelor endoteliale ale capilarelor țesuturilor unde a fost sintetizat. Reglarea secreției este specifică țesutului. În țesutul adipos, sinteza LPL este stimulată de insulină. Aceasta asigură furnizarea de acizi grași pentru sinteza și stocarea sub formă de TAG. În diabetul zaharat, când există un deficit de insulină, nivelurile de LPL scad. Ca urmare, o cantitate mare de LP se acumulează în sânge. În mușchi, unde LPL este implicat în furnizarea de acizi grași pentru oxidarea între mese, insulina inhibă formarea acestei enzime.
Pe suprafața CM, există 2 factori necesari pentru activitatea LPL: apoC-II și fosfolipide. ApoC-II activează această enzimă, iar fosfolipidele sunt implicate în legarea enzimei la suprafața CM. Ca urmare a acțiunii LPL asupra moleculelor TAG, se formează acizi grași și glicerol. Cea mai mare parte a acizilor grași pătrunde în țesuturi, unde pot fi depuse sub formă de TAG (țesut adipos) sau folosiți ca sursă de energie (mușchi). Glicerolul este transportat de sânge către ficat, unde în perioada de absorbție poate fi folosit pentru sinteza grăsimilor.
Ca urmare a acțiunii LPL, cantitatea de grăsimi neutre din CM scade cu 90%, dimensiunea particulelor scade și apoC-II este transferat înapoi la HDL. Particulele rezultate se numesc CM rezidual (rămășițe). Conțin PL, colesterol, vitamine liposolubile, apoB-48 și apoE. CM reziduale sunt captate de hepatocite, care au receptori care interacționează cu aceste apoproteine. Sub acțiunea enzimelor lizozomale, proteinele și lipidele sunt hidrolizate și apoi utilizate. Vitaminele liposolubile și colesterolul exogen sunt folosite în ficat sau transportate în alte organe.
În timpul transportului endogen, TAG și PL resintetizați în ficat sunt incluse în VLDL, care include apoB100 și apoC. VLDL este principala formă de transport pentru TAG endogen. Odată ajuns în sânge, VLDL primește apoC-II și apoE de la HDL și este expus la LPL. În timpul acestui proces, VLDL este mai întâi convertit în LDLP și apoi în LDL. Principala lipide a LDL devine colesterolul, care în compoziția lor este transferat în celulele tuturor țesuturilor. Acizii grași formați în timpul hidrolizei intră în țesuturi, iar glicerolul este transportat de sânge către ficat, unde poate fi din nou utilizat pentru sinteza TAG.
Toate modificările conținutului de medicamente din plasma sanguină, caracterizate prin creșterea, scăderea sau absența lor completă, sunt combinate sub denumirea de dislipoproteinemie. Dislipoproteinemia poate fi fie o manifestare primară specifică a tulburărilor în metabolismul lipidelor și lipoproteinelor, fie un sindrom concomitent în anumite boli ale organelor interne (dislipoproteinemie secundară). Cu tratamentul cu succes al bolii de bază, acestea dispar.
Hipoproteinemia include următoarele afecțiuni.
1. Abetalipoproteinemia apare din cauza unei boli ereditare rare - un defect al genei apoproteinei B, atunci când sinteza proteinelor apoB-100 în ficat și apoB-48 în intestin este perturbată. Ca urmare, CM nu se formează în celulele mucoasei intestinale, iar VLDL nu se formează în ficat, iar picăturile de grăsime se acumulează în celulele acestor organe.
2. Hipobetalipoproteinemie familială: concentrația de medicamente care conțin apoB este de numai 10-15% din nivelul normal, dar organismul este capabil să formeze colesterol.
3. Deficit familial de a-LP (boala Tanger): practic nu se găsește HDL în plasma sanguină, iar în țesuturi se acumulează o cantitate mare de esteri de colesterol;pacienților le lipsește apoC-II, care este un activator al LPL, ceea ce duce la o creștere a concentrației TAG caracteristică acestei afecțiuni în plasma sanguină.
Dintre hiperlipoproteinemiile se disting următoarele tipuri.
Tipul I - hiperchilomicronemia. Rata de îndepărtare a CM din fluxul sanguin depinde de activitatea LPL, prezența HDL, care furnizează apoproteinele C-II și E pentru CM și activitatea de transfer a apoC-II și apoE la CM. Defectele genetice ale oricăreia dintre proteinele implicate în metabolismul CM conduc la dezvoltarea hiperchilomicronemiei familiale - acumularea CM-urilor în sânge. Boala se manifestă în copilăria timpurie și se caracterizează prin hepatosplenomegalie, pancreatită și dureri abdominale. Ca simptom secundar, se observă la pacienții cu diabet zaharat, sindrom nefrotic, hipotiroidism și, de asemenea, cu abuz de alcool. Tratament: dieta saraca in lipide (pana la 30 g/zi) si bogata in carbohidrati.
Tipul II – hipercolesterolemie familială (hiper-b-lipoproteinemie). Acest tip este împărțit în 2 subtipuri: IIa, caracterizat printr-un nivel ridicat de LDL în sânge și IIb, cu niveluri crescute atât de LDL, cât și de VLDL. Boala este asociată cu afectarea recepției și catabolismul LDL (defect al receptorilor celulari pentru LDL sau modificări ale structurii LDL), însoțite de creșterea biosintezei colesterolului, apo-B și LDL. Aceasta este cea mai gravă patologie în metabolismul medicamentelor: riscul de apariție a bolii coronariene la pacienții cu acest tip de tulburare crește de 10-20 de ori față de indivizii sănătoși. Ca fenomen secundar, hiperlipoproteinemia de tip II se poate dezvolta cu hipotiroidism și sindrom nefrotic. Tratament: Dieta saraca in colesterol si grasimi saturate.
Tipul III - dis-b-lipoproteinemia (betalipoproteinemia de bandă largă) este cauzată de o compoziție anormală a VLDL. Sunt îmbogățiți cu colesterol liber și apo-E defect, care inhibă activitatea lipazei TAG hepatice. Acest lucru duce la tulburări în catabolismul colesterolului și VLDL. Boala se manifestă la vârsta de 30-50 de ani. Afecțiunea se caracterizează printr-un conținut ridicat de reziduuri VLDL, hipercolesterolemie și triacilglicerolemie, xantoame, leziuni aterosclerotice ale vaselor periferice și coronare. Tratament: dieteterapie care vizează pierderea în greutate.
Tipul IV – hiperpre-b-lipoproteinemie (hipertriacilglicerolemie). Varianta primară se datorează scăderii activității LPL; o creștere a nivelului de TAG în plasma sanguină are loc datorită fracției VLDL; nu se observă acumularea de CM. Apare numai la adulți și se caracterizează prin dezvoltarea aterosclerozei, mai întâi a arterelor coronare, apoi a arterelor periferice. Boala este adesea însoțită de scăderea toleranței la glucoză. Ca o manifestare secundară, apare în pancreatită și alcoolism. Tratament: dieteterapie care vizează pierderea în greutate.
Tip V – hiperpre-b-lipoproteinemie cu hiperchilomicronemie. Cu acest tip de patologie, modificările fracțiilor lipidice din sânge sunt complexe: conținutul de colesterol și VLDL este crescut, severitatea fracțiilor LDL și HDL este redusă. Pacienții sunt adesea supraponderali; se pot dezvolta hepatosplenomegalie și pancreatită; ateroscleroza nu se dezvoltă în toate cazurile. Ca fenomen secundar, hiperlipoproteinemia de tip V poate fi observată în diabetul zaharat insulino-dependent, hipotiroidism, pancreatită, alcoolism și glicogenoză de tip I. Tratament: dieteterapie care vizează pierderea în greutate, o dietă săracă în carbohidrați și grăsimi.
După absorbția în epiteliul intestinal acizi grași liberi iar 2-monogliceridele formează din nou trigliceride și, împreună cu fosfolipidele și colesterolul, sunt incluse în chilomicroni. Chilomicronii sunt transportați cu fluxul limfatic prin ductul toracic în vena cavă superioară, pătrunzând astfel în fluxul sanguin general.
În interiorul unui chilomicron trigliceride hidrolizat de lipoprotein lipaza, ceea ce duce la eliberarea de acizi grași pe suprafața capilarelor sanguine în țesuturi. Aceasta determină transportul acizilor grași în țesuturi și formarea ulterioară a reziduurilor de chilomicron epuizate în trigliceride. Aceste reziduuri preiau apoi esterii de colesterol din lipoproteinele cu densitate mare, iar particulele sunt absorbite rapid de ficat. Acest sistem de transport pentru acizii grași derivați din alimente se numește sistem de transport exogen.
De asemenea este si sistem de transport endogen, destinat transportului intraorgan al acizilor grași formați chiar în organism. Lipidele sunt transportate de la ficat la țesuturile periferice și înapoi și sunt, de asemenea, transferate din depozitele de grăsime în diferite organe. Transportul lipidelor din ficat la țesuturile periferice implică acțiuni concertate ale VLDL, lipoproteinei cu densitate intermediară (IDL), lipoproteinei cu densitate joasă (LDL) și lipoproteinei cu densitate mare (HDL). Particulele VLDL, ca și chilomicronii, constau dintr-un miez hidrofob mare format din trigliceride și esteri de colesterol și un strat lipidic de suprafață constând în principal din fosfolipide și colesterol.
VLDL sunt sintetizate în ficat, iar depunerea de grăsime în țesuturile periferice este funcția lor principală. Odată ce VLDL intră în sânge, este expus la lipoprotein lipază, care hidrolizează trigliceridele în acizi grași liberi. Acizii grași liberi derivați din chilomicroni sau VLDL pot fi utilizați ca surse de energie, componente structurale ale membranelor fosfolipide sau transformați înapoi în trigliceride și stocați ca atare. Trigliceridele chilomicronilor și VLDL sunt, de asemenea, hidrolizate de lipaza hepatică.
Particule VLDL prin hidroliza trigliceridelor sunt transformate în reziduuri bogate în colesterol și trigliceride (LCR) mai dense, mai mici, care sunt îndepărtate din plasmă de receptorii de lipoproteine hepatice sau pot fi transformate în LDL. LDL este principalul purtător de lipoproteine al colesterolului.
Revenirea din țesuturile periferice la ficat este adesea numită transport invers al colesterolului. Particulele HDL participă la acest proces prin preluarea colesterolului din țesuturi și alte lipoproteine și transportându-l la ficat pentru excreția ulterioară. Un alt tip de transport care există între organe este transferul acizilor grași din depozitele de grăsime către organe pentru oxidare.
Acid gras, obținute în principal ca urmare a hidrolizei trigliceridelor din țesutul adipos, sunt secretate în plasmă, unde se combină cu albumina. Acizii grași legați de albumină sunt transportați de-a lungul unui gradient de concentrație către țesuturile cu metabolism activ, unde sunt utilizați în principal ca surse de energie.
În ultimii 20 de ani, doar câțiva cercetare au fost dedicate problemei transportului lipidelor în perioada perinatală (rezultatele acestor studii nu sunt prezentate în această publicație). Necesitatea unui studiu mai detaliat al acestei probleme este evidentă.
Acizii grași sunt folosiți ca blocuri de construcție material ca parte a lipidelor peretelui celular, ca surse de energie și sunt, de asemenea, stocate „în rezervă” sub formă de trigliceride, în principal în țesutul adipos. Unii LCPUFA omega-6 și omega-3 sunt precursori ai metaboliților bioactivi utilizați în semnalizarea celulară, reglarea genelor și alte sisteme active metabolic.
Întrebare despre rol LCPUFA ARA și DHA în procesul de creștere și dezvoltare a copilului a fost una dintre cele mai importante probleme în cercetările efectuate în domeniul nutriției pediatrice în ultimele două decenii.
Lipidele sunt una dintre componentele principale ale membranelor celulare. O cantitate semnificativă de cercetări în domeniul fiziologiei lipidelor s-a concentrat pe doi acizi grași - ARA și DHA. ARA se găsește în membranele celulare ale tuturor structurilor corpului uman; este un precursor al eicosanoidelor din seria 2, al leucotrienelor din seria 3 și al altor metaboliți care sunt implicați în sistemele de semnalizare celulară și în procesul de reglare a genelor. Cercetările asupra DHA indică adesea rolurile sale structurale și funcționale în membranele celulare.
Acest acid gras găsite în concentrații mari în substanța cenușie a creierului, precum și în tijele și conurile retinei. Studiile privind eliminarea treptată a acizilor grași omega-3 la animale au arătat că LCPUFA omega-6 cu 22 de atomi de carbon (de exemplu, 22:5 n-6) pot înlocui structural, dar nu și funcțional, 22:6 n-3. Cu niveluri inadecvate de 22:6 n-3 în țesuturi, sunt detectate deficiențe vizuale și cognitive. S-a demonstrat că modificarea nivelurilor n-3 din țesut 22:6 afectează funcția neurotransmițătorului, activitatea canalului ionic, căile de semnalizare și expresia genelor.

Reveniți la secțiunea cuprins "
Deoarece lipidele sunt practic molecule hidrofobe, ele sunt transportate în faza apoasă a sângelui ca parte a unor particule speciale - lipoproteine.
Structura lipoproteinelor de transport poate fi comparată cu nuca cine are coajăȘi miez. „Coaja” lipoproteinei este hidrofilă, miezul este hidrofob.
- se formează stratul hidrofil de suprafață fosfolipide(partea lor polară), colesterolul(grupul lui OH), veverite. Hidrofilitatea lipidelor stratului de suprafață este concepută pentru a asigura solubilitatea particulei de lipoproteină în plasma sanguină,
- „miezul” este format din nepolar esteri de colesterol(HS) și triacilgliceroli(TAG), care sunt grăsimi transportate. Raportul lor variază în diferite tipuri de lipoproteine. De asemenea, îndreptate spre centru sunt reziduurile de acizi grași ale fosfolipidelor și partea ciclică a colesterolului.
Schema structurii oricărei lipoproteine de transport
Există patru clase principale de lipoproteine:
- lipoproteine de înaltă densitate (HDL, α-lipoproteine, α-LP),
- lipoproteine cu densitate joasă (LDL, β-lipoproteine, β-LP),
- lipoproteine cu densitate foarte mică (VLDL, pre-β-lipoproteine, pre-β-LP),
- chilomicroni (CM).
Proprietățile și funcțiile lipoproteinelor din diferite clase depind de compoziția lor, adică. asupra tipului de proteine prezente și asupra raportului dintre triacilgliceroli, colesterol și esterii săi, fosfolipide.

Comparația dimensiunii și proprietăților lipoproteinelor
Funcțiile lipoproteinelor
Funcțiile lipoproteinelor din sânge sunt
1. Transfer la celulele țesuturilor și organelor
- acizi grași saturați și mononesaturați din compoziția triacilglicerolilor pentru depozitarea ulterioară sau utilizarea ca substrat energetic;
- acizi grași polinesaturați în esterii de colesterol pentru utilizarea de către celule în sinteza fosfolipidelor sau formarea eicosanoizilor,
- colesterolul ca material membranar,
- fosfolipide ca material membranar,
Chilomicronii și VLDL sunt în primul rând responsabili de transport acizi grași ca parte a TAG. Lipoproteine de înaltă și joasă densitate - pentru transportul liber colesterolulȘi acizi grași ca parte a eterilor săi. HDL este, de asemenea, capabil să doneze celulelor o parte din membrana fosfolipidă.
2. Îndepărtarea excesului de colesterol din membranele celulare.
3. Transportul vitaminelor liposolubile.
4. Transfer de hormoni steroizi (împreună cu proteine de transport specifice).
Apoproteine lipoproteice
Proteinele din lipoproteine sunt de obicei numite apowhites, există mai multe tipuri de ele - A, B, C, D, E. În fiecare clasă de lipoproteine există apoproteine corespunzătoare care își îndeplinesc propria funcție:
1. Structural funcţie(" staționar» proteine) – leagă lipidele și formează complexe proteine-lipide:
- apoB-48– adaugă triacilceroli,
- apoB-100– leagă atât triacilglicerolii, cât și esterii colesterolului,
- apoA-I- acceptă fosfolipide,
- apoA-IV– se leagă de colesterol.
2. Cofactor funcţie(" dinamic» proteine) – afectează activitatea enzimelor metabolice ale lipoproteinelor din sânge.