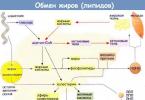
Ресинтезовані в кишечнику ліпіди транспортуються у складі хіломікронів з лімфою. Ліпіди нерозчинні у воді, тому вони транспортуються в асоціації з білками.
Ліпопротеїди – комплекси білків та ліпідів, транспортна форма ліпідів у крові. Ліпіди ЛП: тригліцериди, фосфоліпіди, холестерин. Білки ЛП – апопротеїни окремих класів ЛП.
Функції апопротеїнів - структурна (ЛП), транспортна, секреторна (потрібні для секреції ЛП клітинами печінки та кишечника), необхідні для взаємодії ЛП з рецепторами, активують ферменти, що беруть участь у метаболізмі ЛП, надають ліпідам водорозчинність, апопротеїн А1 ЛПВЩ активує ЛХТ.
Структура ліпопротеїду. Гідрофобне ядро (ефіри холестерину, ТГ) оточене зовні фосфоліпідами, вільним холестерином, апобелками.
Класифікація ЛП.
на підставі рухливості в електричному полі: - ХМ залишаються на старті, - інші мігрують до зон глобулінів: ß-ЛП, пре-ß-ЛП, α-ЛП.
за величиною гідратованої щільності (методом ультрацентрифугування) ЛП ділять на ХМ, ЛПДНЩ, ЛПСШ, ЛПНЩ, ЛПВЩ.
Біологічна роль ЛП. Ендогенні ТГ доставляють у периферичні клітини для забезпечення потреби в енергії, а ендогенний холестерин – для біосинтезу мембран.
Склад та властивості ліпопротеїнів.
Хіломікрони транспортують екзогенні ТГ, холестерин, фосфоліпіди харчові жири з кишечника в тканини через лімфатичну систему. В ентероцитах синтезуються незрілі ХМ, які спочатку потрапляють у лімфу, а потім у кровотік. Основний апопротеїн ХМ – білок В-48 синтезується у клітинах слизової оболонки кишечника, необхідний для формування структури ХМ. У крові незрілі ХМ отримують від ЛПВЩ інші апобелки - С-і Е-і перетворюються на зрілі ХМ. Першим органом, через який мають пройти ХМ, є легкі. При надходженні ХМ з кишечника в кров відбувається активація опасистих клітин з виходом гепарину та активацією ліпопротеїнліпази.
Адсорбтивна ліпемія – підвищення кількості ліпідів у крові, що настає після прийому їжі.
Ліпопротеїдліпаза (просвітлюючий фактор) гідролізує ТАГ у ХМ та ЛПДНЩ, знаходиться в ендотелії капілярів різних органів, активується гепарином та збільшенням у крові ТАГ. ТАГ хіломікронів розщеплюються на поверхні та всередині гепатоцитів, на поверхні ендотелію капілярів жирової тканини.
ЛПДНЩ і ЛПВЩ - секретуються в кров печінкою, де здійснюється їх синтез. ЛПНЩ утворюються в кровотоку з ЛПДНЩ в результаті гідролізу частини ТГ ЛПДНЩ ліпопротеїдліпазою.
Доля ЛПНГ. На плазматичних мембранах клітин є рецептори ЛПНЩ. ЛПНЩ проникають у клітини, де під впливом гідролаз лізосом розпадаються на складові компоненти, вільний холестерин включається до складу плазматичної мембрани або етерифікується та у вигляді ефірів відкладається в цитоплазмі. Можливий неспецифічний ендоцитоз ЛПНЩ.
ЛПВЩ виносять холестерин у печінку. У печінці холестерин окислюється у жовчні кислоти та видаляється через кишечник. Окислення холестерину відбувається у печінці монооксигеназною системою. 7а-гідроксилаза холестерину – лімітуючий фермент. ЛПВЩ здатні акцептувати холестерин з клітинних мембран.
Перетворення вільного холестерину на естерифікований: холестерин + лецитин → лізолецитин + складний ефір холестерину. Ефір холестерину утворюється на поверхні ЛПВЩ і переноситься в ядро ЛПВЩ.
Зниження холестерину ЛПВЩ у плазмі крові пов'язане зі зниженням ЛХАТ, кількості частинок ЛПЗЩ, лецитину, апопротеїну А1.
Період напіврозпаду. ХМ – менше години, ЛПДНЩ – 2-4 години, ЛПНЩ – 2-4 доби, ЛПВЩ – 5 діб. ЛНП та ЛВП поглинаються шляхом ендоцитозу клітинами печінки, кишечника, жирової тканини, нирок, надниркових залоз та руйнуються в лізосомах.
Неестерифіковані жирні кислоти (НЕЖК). Жирні кислоти в плазмі знаходяться в естерифікованій формі: у складі фосфоліпідів, ефірів холестерину, моно-, ді-, тригліцеридів. У вільному вигляді жирні кислоти транспортуються в плазмі з жирової тканини та печінки до скелетних м'язів, у цьому випадку вони пов'язані з альбуміном.
НЕЖК надходять у плазму крові в результаті ліполізу ТГ, що каталізується ліпазою в жировій тканині, утворюються при дії ліпопротеїдліпази на ТГ плазми крові в період переходу їх у тканини, жирні кислоти з довжиною ланцюга менше 1о атомів вуглецю всмоктуються в неестерифікованій формі через систему портального в печінку (це важливо для дітей, оскільки молоко багате на жирні кислоти з коротким ланцюгом).
Триацилгліцериди – транспортна форма для насичених жирних кислот. Фосфоліпіди та холестерин – транспортна форма для поліненасичених жирних кислот.
Функції НЕЖК – дають 50% енергії при голодуванні, енергетичний матеріал для міокарда, м'язів, нирок, печінки, насичені жирні кислоти виконують енергетичну, а ненасичені – пластичну функції.
Відповідь. У крові хворого підвищується аміак, глутамін, іон амонію NH 4 + .
Транспорт ліпідів в організмі йде двома шляхами:
- 1) жирні кислоти транспортуються у крові за допомогою альбумінів;
- 2) ТГ, ФО, ХС, ЕХС та д.р. ліпіди транспортуються у крові у складі ліпопротеїнів.
Обмін ліпопротеїнів
Ліпопротеїни (ЛП) – це надмолекулярні комплекси сферичної форми, що складаються з ліпідів, білків та вуглеводів. ЛП мають гідрофільну оболонку та гідрофобне ядро. У гідрофільну оболонку входять білки та амфіфільні ліпіди – ФО, ХС. У гідрофобне ядро входять гідрофобні ліпіди – ТГ, ефіри ХС тощо. ЛП добре розчиняються у воді.
В організмі синтезуються кілька видів ЛП, вони відрізняються хімічним складом, утворюються у різних місцях та здійснюють транспорт ліпідів у різних напрямках.
ЛП поділяють за допомогою:
- 1) електрофорезу, за зарядом та розміром, на б-ЛП, в-ЛП, пре-в-ЛП та ХМ;
- 2) центрифугування, за щільністю, на ЛПВЩ, ЛПНЩ, ЛПСП, ЛПДНЩ і ХМ.
Співвідношення та кількість ЛП у крові залежить від часу доби та від харчування. У постабсорбтивний період та при голодуванні в крові присутні лише ЛПНГ та ЛПВЩ.
Основні види ліпопротеїнів
Склад, % ХМ ЛПДНЩ
- (пре-в-ЛП) ЛПВП
- (пре-в-ЛП) ЛПНГ
- (в-ЛП) ЛПВЩ
- (Б-ЛП)
Білки 2 10 11 22 50
ФО 3 18 23 21 27
ЕХС 3 10 30 42 16
ТГ 85 55 26 7 3
Щільність, г/мл 0,92-0,98 0,96-1,00 0,96-1,00 1,00-1,06 1,06-1,21
Діаметр, нм >120 30-100 30-100 21-100 7-15
Функції Транспорт до тканин екзогенних ліпідів їжі Транспорт до тканин ендогенних ліпідів печінки Транспорт до тканин ендогенних ліпідів печінки Транспорт ХС
у тканині Видалення надлишку ХС
з тканин
апо А, С, Е
Місце утворення ентероцит гепатоцит в крові з ЛПДНЩ в крові з ЛППП гепатоцит
Апо В-48, С-II, Е В-100, С-II, Е В-100, Е-100 А-I С-II, Е, D
Норма у крові< 2,2 ммоль/л 0,9- 1,9 ммоль/л
Апобілки
Білки, що входять до складу ЛП, називаються апопротеїни (апобілки, апо). До найпоширеніших апопротеїнів відносять: апо А-I, А-II, В-48, В-100, С-I, С-II, С-III, D, Е. Апобілки можуть бути периферичними (гідрофільні: А-II, С-II, Е) та інтегральними (мають гідрофобну ділянку: В-48, В-100). Периферичні апо переходять між ЛП, а інтегральні – ні. Апопротеїни виконують кілька функцій:
Апобелок Функція Місце освіти Локалізація
А-I Активатор ЛХАТ, освіта ЕХС печінка ЛПВЩ
А-II Активатор ЛХАТ, освіта ЕХС ЛПВЩ, ХМ
В-48 Структурна (синтез ЛП), рецепторна (фагоцитоз ЛП) ентероцит ХМ
В-100 Структурна (синтез ЛП), рецепторна (фагоцитоз ЛП) печінка ЛПДНЩ, ЛПСШ, ЛПНЩ
С-I Активатор ЛХАТ, освіта ЕХС Печінка ЛПВЩ, ЛПДНЩ
С-II Активатор ЛПЛ, стимулює гідроліз ТГ в ЛП Печінка ЛПВЩ > ХМ, ЛПДНЩ
С-III Інгібітор ЛПЛ, інгібує гідроліз ТГ в ЛП Печінка ЛПВЩ > ХМ, ЛПДНЩ
D Перенесення ефірів холестерину (БПЕХ) Печінка ЛПВЩ
Е Рецепторна, фагоцитоз ЛП печінка ЛПВЩ > ХМ, ЛПДНЩ, ЛППП
Ферменти транспорту ліпідів
Ліпопротеїнліпаза (ЛПЛ) (КФ 3.1.1.34, ген LPL, близько 40 дефектних алелів) пов'язана з гепарансульфатом, що знаходиться на поверхні ендотеліальних клітин капілярів кровоносних судин. Вона гідролізує ТГ у складі ЛП до гліцерину та 3 жирних кислот. При втраті ТГ, ХМ перетворюються на залишкові ХМ, а ЛПДНЩ підвищують свою щільність до ЛПСШ та ЛПНЩ.
Апо С-II ЛП активує ЛПЛ, а фосфоліпіди ЛП беруть участь у зв'язуванні ЛПЛ із поверхнею ЛП. Синтез ЛПЛ індукується інсуліном. АПО С-ІІІ інгібує ЛПЛ.
ЛПЛ синтезується в клітинах багатьох тканин: жирової, м'язової, в легенях, селезінці, клітинах молочної залози, що лактує. Її немає у печінці. Ізоферменти ЛПЛ різних тканин відрізняються значенням Кm. У жировій тканині ЛПЛ має Кm у 10 разів більше, ніж у міокарді, тому в жирову тканину поглинає жирні кислоти тільки при надлишку ТГ у крові, а міокард – постійно, навіть за низької концентрації ТГ у крові. Жирні кислоти в адипоцитах застосовуються для синтезу ТГ, в міокарді як джерело енергії.
Печінкова ліпаза знаходиться на поверхні гепатоцитів, вона не діє на зрілі ХМ, а гідролізує ТГ у ЛПСШ.
Лецитин: холестерол-ацил-трансфераза (ЛХАТ) перебуває у ЛПВЩ, вона переносить ацил з лецитину на ХС з утворенням ЕХС та лізолецитину. Її активують АПО А-I, А-II і С-I.
лецитин + ХС > лізолецітин + ЕХС
ЕХС занурюється в ядро ЛПВЩ або переноситься за участю АПО D на інші ЛПЗ.
Рецептори транспорту ліпідів
Рецептор ЛПНГ - складний білок, що складається з 5 доменів і містить вуглеводну частину. Рецептор ЛПНГ взаємодіє з білками ano B-100 і апо Е, добре зв'язує ЛПНГ, гірше за ЛППП, ЛПДНЩ, залишкові ХМ, що містять ці апо. Клітини тканин містять велику кількість рецепторів ЛПНЩ на своїй поверхні. Наприклад, однією клітині фібробласта є від 20 000 до 50 000 рецепторів.
Якщо кількість холестеролу, що надходить у клітину, перевищує її потребу, синтез рецепторів ЛПНГ пригнічується, що зменшує потік холестеролу з крові в клітини. При зниженні концентрації вільного холестеролу в клітині, навпаки, активується синтез ГМГ-КоА-редуктази та рецепторів ЛПНЩ. Стимулюють синтез рецепторів ЛПНГ гормони: інсулін та трийодтиронін (Т3), статеві гормони, а глюкокортикоїди – зменшують.
Білок, подібним до рецептора ЛПНЩ на поверхні клітин багатьох органів (печінки, мозку, плаценти) є інший тип рецептора, званий «білком, подібним до рецептора ЛПНЩ». Цей рецептор взаємодіє з апо Е і захоплює ремнантні (залишкові) ХМ та ЛПСШ. Так як ремнантні частинки містять холестерину, цей тип рецепторів також забезпечує надходження його в тканини.
Крім надходження холестерину в тканини шляхом ендоцитозу ЛП, деяка кількість холестерину надходить у клітини шляхом дифузії з ЛПНЩ та інших ЛП при їх контакті з мембранами клітин.
У крові в нормі концентрація:
- * ЛПНЩ
- * загальних ліпідів 4-8г/л,
- * ТГ 0,5-2,1 ммоль/л,
- * Вільних жирних кислот 400-800 мкмоль/л
Ліпіди у водному середовищі нерозчинні, тому їхнього транспорту в організмі утворюються комплекси ліпідів з білками – ліпопротеїни (ЛП). Розрізняють екзо- та ендогенний транспорт ліпідів. До екзогенного відносять транспорт ліпідів, що надійшли з їжею, а до ендогенного – переміщення ліпідів, синтезованих в організмі.
Існує кілька типів ЛП, але всі вони мають подібну будову – гідрофобне ядро та гідрофільний шар на поверхні. Гідрофільний шар утворений білками, які називають апопротеїнами, та амфіфільними молекулами ліпідів – фосфоліпідами та холестеролом. Гідрофільні групи цих молекул звернені до водної фази, а гідрофобні - до ядра, в якому знаходяться ліпіди, що транспортуються. Апопротеїни виконують кілька функцій:
· Формують структуру ліпопротеїнів (наприклад, В-48 - основний білок ХМ, В-100 - основний білок ЛПДНЩ, ЛПСШ, ЛПНЩ);
· Взаємодіють з рецепторами на поверхні клітин, визначаючи, якими тканинами буде захоплюватися даний тип ліпопротеїнів (апопротеїн В-100, Е);
· Є ферментами або активаторами ферментів, що діють на ліпопротеїни (С-II – активатор ЛП-ліпази, А-I – активатор лецитин: холестеролацилтрансферази).
При екзогенному транспорті ресинтезовані в ентероцитах ТАГ разом з фосфоліпідами, холестеролом та білками утворюють ХМ, і в такому вигляді секретуються спочатку у лімфу, а потім потрапляють у кров. У лімфі та крові з ЛПВЩ на ХМ переносяться апопротеїни Е (апо Е) та С-II (апо С-II), таким чином ХМ перетворюються на «зрілі». ХМ мають досить великий розмір, тому після прийому жирної їжі вони надають плазмі крові опалесцентний, схожий на молоко, вид. Потрапляючи в систему кровообігу, ХМ швидко піддаються катаболізму і зникають протягом декількох годин. Час руйнування ХМ залежить від гідролізу ТАГ під дією ліпопротеїнліпази (ЛПЛ). Цей фермент синтезується та секретується жировою та м'язовою тканинами, клітинами молочних залоз. Секретована ЛПЛ пов'язується з поверхнею ендотеліальних клітин капілярів тканин, де вона синтезувалася. Регуляція секреції має тканинну специфічність. У жировій тканині синтез ЛПЛ стимулюється інсуліном. Тим самим забезпечується надходження жирних кислот для синтезу та зберігання у вигляді ТАГ. При цукровому діабеті, коли спостерігається дефіцит інсуліну, рівень ЛПЛ знижується. В результаті в крові накопичується велика кількість ЛЗ. У м'язах, де ЛПЛ бере участь у постачанні жирних кислот для окислення між їдою, інсулін пригнічує утворення цього ферменту.
На поверхні ХМ розрізняють 2 фактори, необхідні активності ЛПЛ – апоС-II і фосфоліпіди. АпоС-II активує цей фермент, а фосфоліпіди беруть участь у зв'язуванні ферменту з поверхнею ХМ. Внаслідок дії ЛПЛ на молекули ТАГ утворюються жирні кислоти та гліцерол. Основна маса жирних кислот проникає в тканини, де може депонуватися у вигляді ТАГ (жирова тканина) або використовувати як джерело енергії (м'язи). Гліцерол транспортується кров'ю до печінки, де в абсорбтивний період може бути використаний для синтезу жирів.
В результаті дії ЛПЛ кількість нейтральних жирів у ХМ знижується на 90%, зменшуючи розміри частинок, апоС-II переноситься назад на ЛПВЩ. Частки, що утворилися, називаються залишковими ХМ (ремнантами). Вони містять ФО, ХС, жиророзчинні вітаміни, апоВ-48 та апоЕ. Залишкові ХМ захоплюються гепатоцитами, які мають рецептори, що взаємодіють із цими апопротеїнами. Під дією ферментів лізосом білки та ліпіди гідролізуються, а потім утилізуються. Жиророзчинні вітаміни та екзогенний холестерин використовуються в печінці або транспортуються в інші органи.
При ендогенному транспорті ресинтезовані в печінці ТАГ та ФО включаються до складу ЛПДНЩ, куди входять апоВ100 і апоС. ЛПОНП є основною транспортною формою для ендогенних ТАГ. Потрапивши в кров, ЛПДНЩ отримують апоС-II і апоЕ від ЛПЗЩ і піддаються дії ЛПЛ. У ході цього процесу ЛПДНЩ спочатку перетворюються на ЛПНЩ, а потім в ЛПНЩ. Основним ліпідом ЛПНГ стає ХС, який у їхньому складі переноситься до клітин усіх тканин. Утворені в ході гідролізу жирні кислоти надходять у тканини, а гліцерол кров'ю транспортується до печінки, де знову може використовуватися для синтезу ТАГ.
Усі зміни вмісту ЛП у плазмі крові, що характеризуються їх підвищенням, зниженням або повною відсутністю, поєднують під назвою дисліпопротеїнемій. Дисліпопротеїнемія може бути або специфічним первинним проявом порушень в обміні ліпідів та ліпопротеїнів, або супутнім синдромом при деяких захворюваннях внутрішніх органів (вторинні дисліпопротеїнемії). За успішного лікування основного захворювання вони зникають.
До гіполіпопротеїнемій відносять такі стани.
1. Абеталіпопротеїнемія виникає при рідкісному спадковому захворюванні – дефект гена апопротеїну В, коли порушується синтез білків апоВ-100 у печінці та апоВ-48 у кишечнику. У результаті клітинах слизової оболонки кишечника не формуються ХМ, а печінки – ЛПОНП, й у клітинах цих органів накопичуються крапельки жиру.
2. Сімейна гіпобеталіпопротеїнемія: концентрація ЛП, що містять апоВ, становить лише 10-15% нормального рівня, але організм здатний утворювати ХМ.
3. Сімейна недостатність a-ЛП (хвороба Тангіра): у плазмі крові практично не виявляються ЛПВЩ, а в тканинах накопичується велика кількість ефірів ХС, у пацієнтів відсутня апоС-II, що є активатором ЛПЛ, що веде до характерного для даного стану підвищення концентрації ТАГ у плазмі крові.
Серед гіперліпопротеїнемій розрізняють такі типи.
Тип I – гіперхіломікронемія. Швидкість видалення ХМ із кровотоку залежить від активності ЛПЛ, присутності ЛПВЩ, що постачають апопротеїни С-II та Е для ХМ, активності перенесення апоС-II та апоЕ на ХМ. Генетичні дефекти будь-якого з білків, що беруть участь у метаболізмі ХМ, призводять до розвитку сімейної гіперхіломікронемії – накопичення ХМ у крові. Захворювання проявляється у ранньому дитинстві, характеризується гепатоспленомегалією, панкреатитом, абдомінальними болями. Як вторинна ознака спостерігається у хворих на цукровий діабет, нефротичним синдромом, гіпотиреозом, а також при зловживанні алкоголем. Лікування: дієта з низьким вмістом ліпідів (до 30 г/добу) та високим вмістом вуглеводів.
Тип II - сімейна гіперхолестеролемія (гіпер-b-ліпопротеїнемія). Цей тип ділять на 2 підтипи: IIа, що характеризується високим вмістом у крові ЛПНГ, і IIб - з підвищеним рівнем як ЛПНГ, так і ЛПДНЩ. Захворювання пов'язане з порушенням рецепції та катаболізму ЛПНЩ (дефект клітинних рецепторів для ЛПНЩ або зміна структури ЛПНЩ), супроводжується посиленням біосинтезу холестеролу, апо-В та ЛПНЩ. Це найбільш серйозна патологія в обміні ЛП: ступінь ризику розвитку ІХС у пацієнтів із цим типом порушення зростає у 10-20 разів у порівнянні зі здоровими особами. Як вторинне явище гіперліпопротеїнемія ІІ типу може розвиватися при гіпотиреозі, нефротичному синдромі. Лікування: дієта з низьким вмістом холестеролу та насичених жирів.
Тип III – дис-b-ліпопротеїнемія (широкополосна беталіпопротенемія) обумовлена аномальним складом ЛПДНЩ. Вони збагачені вільним ХС та дефектним апо-Е, що гальмує активність печінкової ТАГ-ліпази. Це веде до порушень катаболізму ХМ та ЛПДНЩ. Захворювання проявляється у віці 30-50 років. Стан характеризується високим вмістом залишків ЛПДНЩ, гіперхолестеролемією та триацилгліцеролемією, спостерігаються ксантоми, атеросклеротичні ураження периферичних та коронарних судин. Лікування: дієтотерапія, спрямована на зниження ваги.
Тип IV – гіперпре-b-ліпопротеїнемія (гіпертріацилгліцеролемія). Первинний варіант обумовлений зменшенням активності ЛПЛ, підвищення рівня ТАГ у плазмі крові відбувається за рахунок фракції ЛПДНЩ, акумуляції ХМ при цьому не спостерігається. Зустрічається лише в дорослих, характеризується розвитком атеросклерозу спочатку коронарних, потім периферичних артерій. Захворювання часто супроводжується зниженням толерантності до глюкози. Як вторинне прояв трапляється при панкреатиті, алкоголізмі. Лікування: дієтотерапія, спрямована на зниження ваги.
Тип V – гіперпре-b-ліпопротеїнемія з гіперхіломікронемією. При цьому типі патології зміни фракцій ЛП крові носять складний характер: підвищено вміст ХМ та ЛПДНЩ, вираженість фракцій ЛПНЩ та ЛПЗЩ зменшена. Хворі часто мають надмірну масу тіла, можливий розвиток гепатоспленомегалії, панкреатиту, атеросклероз розвивається не у всіх випадках. Як вторинне явище гіперліпопротеїнемія V типу може спостерігатися при інсулінзалежному цукровому діабеті, гіпотиреозі, панкреатиті, алкоголізмі, глікогенозі І типу. Лікування: дієтотерапія, спрямована на зниження ваги, дієта з невисоким вмістом вуглеводів та жирів.
Після всмоктування в епітелій кишки вільні жирні кислотиі 2-моногліцериди знову утворюють тригліцериди і разом з фосфоліпідами і холестеролом включаються в хіломікрони. Хіломікрони транспортуються зі струмом лімфи через грудну протоку у верхню порожню вену, потрапляючи таким чином в загальний кровотік.
Усередині хіломікрону тригліцеридигідролізуються ліпопротеїнліпазою, що призводить до вивільнення жирних кислот на поверхні кровоносних капілярів у тканинах. Це зумовлює транспорт жирних кислот у тканини та подальше утворення залишків хіломікронів, збіднених тригліцеридами. Ці залишки потім забирають холестеролові ефіри з ліпопротеїнів високої щільності, і частинки швидко захоплюються печінкою. Цю систему транспорту жирних кислот харчового походження називають екзогенною транспортною системою.
Також існує ендогенна транспортна системапризначена для внутрішньоорганного транспорту жирних кислот, утворених у самому організмі. Ліпіди транспортуються з печінки до периферичних тканин і назад, а також переносяться з жирових депо до різних органів. Транспорт ліпідів від печінки до периферичних тканин включає узгоджені дії ЛПДНЩ, ліпопротеїнів проміжної щільності (ЛППП), ліпопротеїнів низької щільності (ЛПНЩ) та ліпопротеїнів високої щільності (ЛПЗЩ). Частинки ЛПДНЩ подібно до хіломікронів складаються з великого гідрофобного ядра, утвореного тригліцеридами і ефірами холестеролу, і поверхневого ліпідного шару, що складається в основному з фосфоліпідів і холестеролу.
ЛПДНЩсинтезуються в печінці, і відкладення жиру в периферичних тканинах є основною функцією. Після потрапляння в кровотік ЛПДНЩ піддаються впливу ліпопротеїнліпази, що гідролізує тригліцериди до вільних жирних кислот. Вільні жирні кислоти, що походять з хіломікронів або ЛПДНЩ, можуть бути використані як джерела енергії, структурних компонентів фосфоліпідних мембран або перетворюватися назад на тригліцериди і в такому вигляді зберігатися. Тригліцериди хіломікронів і ЛПДНЩ також піддаються гідролізу ліпази печінки.
Частинки ЛПДНЩза допомогою гідролізу тригліцеридів перетворюються на більш щільні, менші за розміром холестерол- та тригліцерид-збагачені залишки (ЛПСШ), які видаляються з плазми за допомогою рецепторів печінкових ліпопротеїнів або можуть бути перетворені на ЛПНЩ. ЛПНГ є основними ліпопротеїнами-переносниками холестеролу.
Повернення з периферичних тканин до печінки часто називають зворотним транспортом холестеролу. Частинки ЛПВЩ беруть участь у цьому процесі, забираючи холестерол з тканин та інших ліпопротеїнів і переносячи його в печінку для подальшої екскреції. Ще один вид транспортування, що існує між органами, - перенесення жирних кислот з жирових депо до органів окиснення.
Жирні кислоти, одержувані переважно в результаті гідролізу тригліцеридів жирової тканини, секретуються в плазму, де з'єднуються з альбуміном. Пов'язані з альбуміном жирні кислоти переносяться по градієнту концентрації в тканині з активним метаболізмом, де використовуються переважно як джерела енергії.
Протягом останніх 20 років лише кілька дослідженьбули присвячені питанню транспорту ліпідів у перинатальному періоді (результати цих досліджень у цьому виданні не представлені). Очевидною є необхідність більш детального вивчення цієї проблеми.
Жирні кислоти використовуються як будівельний матеріалуу складі ліпідів клітинної стінки, як джерела енергії, а також відкладаються «про запас» у вигляді тригліцеридів переважно в жировій тканині. Деякі омега-6 та омега-3 ДЦПНЖК є попередниками біологічно активних метаболітів, що використовуються у сигнальній системі клітин, регуляції генів та інших метаболічно активних системах.
Питання про роль ДЦПНЖК ARA та DHA у процесі зростання та розвитку дитини є одним з найважливіших питань у дослідженнях, що проводяться в галузі дитячої нутриціології протягом останніх двох десятиліть.
Ліпідиє одним із основних компонентів клітинних мембран. Значна кількість досліджень у галузі фізіології ліпідів присвячена двом жирним кислотам – ARA та DHA. ARA виявлено у складі клітинних мембран всіх структур організму людини; вона є попередником ейкозаноїдів 2-ї серії, лейкотрієнів 3-ї серії та інших метаболітів, які включені в сигнальні системи клітин та процес генної регуляції. Дослідження, присвячені DHA, часто вказують на її структурну та функціональну роль у складі клітинних мембран.
Ця жирна кислотавиявлена у високій концентрації в сірій речовині головного мозку, а також у паличках та колбочках сітківки. Дослідження поступового вилучення з дієти тварин омега-3 жирних кислот показали, що містять 22 атоми вуглецю омега-6 ДЦПНЖК (наприклад, 22:5 п-6) здатні структурно, але не функціонально замінити 22:6 n-3. При неадекватному рівні 22:6 n-3 у тканинах виявляються порушення зору та пізнавальних здібностей. Було показано, що зміна вмісту 22:6 n-3 у тканинах впливає на нейротрансмітерну функцію, активність іонних каналів, сигнальні шляхи та експресію генів.

Повернутись до змісту розділу "
Оскільки ліпіди є основою своєї гидрофобными молекулами, всі вони транспортуються у водної фазі крові у складі особливих частинок – ліпопротеїнів .
Структуру транспортних ліпопротеїнів можна порівняти з горіхом, у яких є шкаралупаі ядро. "Шкаралупа" ліпопротеїну є гідрофільною, ядро - гідрофобне.
- поверхневий гідрофільний шар формують фосфоліпіди(їхня полярна частина), холестерол(його ВІН-група), білки. Гідрофільність ліпідів поверхневого шару покликана забезпечити розчинність ліпопротеїнової частки у плазмі,
- "ядро" формують неполярні ефіри холестеролу(ХС) та триацилгліцероли(ТАГ), які і є жирами, що транспортуються. Їх співвідношення коливається у різних типах ліпопротеїнів. Також до центру звернені жирнокислотні залишки фосфоліпідів та циклічна частина холестеролу.
Схема будови будь-якого транспортного ліпопротеїну
Виділяють чотири основні класи ліпопротеїнів:
- ліпопротеїни високої щільності (ЛПЗЩ, α-ліпопротеїни, α-ЛП),
- ліпопротеїни низької щільності (ЛПНЩ, β-ліпопротеїни, β-ЛП),
- ліпопротеїни дуже низької щільності (ЛПДНЩ, пре-β-ліпопротеїни, пре-β-ЛП),
- хіломікрони (ХМ).
Властивості та функції ліпопротеїнів різних класів залежить від їх складу, тобто. від виду присутніх білків та від співвідношення триацилгліцеролів, холестеролу та його ефірів, фосфоліпідів.

Порівняння розміру та властивостей ліпопротеїнів
Функції ліпопротеїнів
Функціями ліпопротеїнів крові є
1. Перенесення до клітин тканин та органів
- насичених і мононенасичених жирних кислот у складі триацилгліцеролів для подальшого депонування або використання як енергетичні субстрати,
- поліненасичених жирних кислот у складі ефірів холестеролу для використання клітинами в синтезі фосфоліпідів або утворення ейкозаноїдів
- холестеролу в якості мембранного матеріалу,
- фосфоліпідів як мембранний матеріал,
Хіломікрони та ЛПДНЩ відповідальні, в першу чергу, за транспорт жирних кислоту складі ТАГ. Ліпопротеїни високої та низької щільності – за транспорт вільного холестеролуі жирних кислоту складі його ефірів. ЛПВЩ здатні також віддавати клітинам частину своєї фосфоліпідної оболонки.
2. Видалення надлишку холестеролу з мембран клітин.
3. Транспорт жиророзчинних вітамінів.
4. Перенесення стероїдних гормонів (поряд із специфічними транспортними білками).
Апобілки ліпопротеїнів
Білки у ліпопротеїнах зазвичай називаються апобілками, виділяють кілька типів – А, У, З, D, Е. У кожному класі ліпопротеїнів перебувають відповідні йому апобелки, виконують свою власну функцію:
1. Структурнафункція (« стаціонарні» білки) – зв'язують ліпіди та формують білок-ліпідні комплекси:
- апоВ-48– приєднує триациліцероли,
- апоВ-100– пов'язує як триацилгліцероли, так і ефіри холестерину,
- апоА-I- акцептує фосфоліпіди,
- апоА-IV– зв'язується із холестеролом.
2. Кофакторнафункція (« динамічнібілки) – впливають на активність ферментів метаболізму ліпопротеїнів у крові.