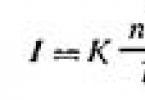Текст роботи розміщено без зображень та формул.
Повна версія роботи доступна у вкладці "Файли роботи" у форматі PDF
Кожен з нас у своєму повсякденному житті не раз стикався і стикається зі звичайними з одного боку, але разом з тим дивовижними з іншого боку явищами, зовсім не замислюючись при цьому, з якими чудовими фізичними явищами має справу.
У майбутньому я хотіла б пов'язати своє життя з такою наукою як фізика, тому вже зараз цікавлюся будь-якими питаннями з цього предмета і вибрала як тему свого дослідження один із оптичних ефектів.
Сьогодні існують роботи, присвячені оптичним ефектам, зокрема, ефекту Тиндаля. Однак я вирішила вивчити цю тему шляхом проведення експерименту на власному досвіді.
Чому при пропусканні через каламутне скло, задимлене повітря чи розчин крохмалю світла різного спектрального забарвлення ми спостерігаємо різний результат? Чому густий туман чи купчасті хмари здаються нам білими, а серпанок від лісових пожеж – блакитно-фіолетовий. Спробуємо пояснити цим явищам.
Мета проекту:
виявити колоїди за допомогою ефекту Тіндаля;
дослідити вплив факторів, що визначають проходження світлового пучка через колоїдний розчин.
Завдання дослідження:
дослідження впливу довжини хвилі на ефект Тиндаля;
дослідження впливу розміру частинок на ефект Тиндаля;
дослідження впливу концентрації частинок на ефект Тиндаля;
пошук додаткової інформації щодо ефекту Тіндаля;
узагальнення отриманих знань.
Ефект Тіндаля
Заломлення світла, відображення, дисперсія, інтерференція, дифракція та багато іншого: оптичні ефекти оточують нас усюди. Один із них — ефект Тіндаля, відкритий англійським фізиком Джоном Тіндалем.
Джон Тіндал — геодезист, співробітник Фарадея, директор Королівського інституту в Лондоні, гляціолог і оптик, акустик і фахівець з магнетизму. Його прізвище дало назву кратеру на Місяці, льодовику в Чилі та цікавому оптичному ефекту.
Ефект Тіндаля - це світіння оптично неоднорідного середовища внаслідок розсіювання світла, що проходить через неї. Дане явище обумовлено дифракцією світла на окремих частинках або елементах неоднорідності середовища, розмір яких набагато менше довжини хвилі світла, що розсіюється.
Що ж таке неоднорідне середовище? Неоднорідне середовище - середовище, що характеризується непостійністю показника заломлення. Тобто. n ≠const.
Яку характерну рису цього ефекту можна виділити? Ефект Тіндаля характерний для колоїдних систем (систем, в яких одна речовина у вигляді частинок різної величини розподілена в іншому. Наприклад, гідрозолей, тютюнового диму, туману, гелю і т.д.) з низькою концентрацією частинок, що мають показник заломлення, відмінний від показника заломлення середовища. Зазвичай спостерігається у вигляді світлого конуса на темному тлі (конус Тіндаля) при пропусканні фокусованого світлового пучка збоку через скляну посудину з плоскопаралельними стінками, заповнений колоїдним розчином. (Колоїдні розчини - це високодисперсні двофазні системи, що складаються з дисперсійного середовища та дисперсної фази, причому лінійні розміри частинок останньої лежать в межах від 1 до 100 нм).
Ефект Тіндаля по суті те саме, що опалесценція (різке посилення розсіювання світла). Але традиційно перший термін відносять до інтенсивного розсіювання світла в обмеженому просторі по ходу променя, а другий - до слабкого розсіювання світла всім обсягом об'єкта, що спостерігається.
Експериментальна робота
Використовуючи просту методику, ми побачимо, як за допомогою ефекту Тіндаля можна виявити колоїдні системи рідин.
Матеріали: 2 скляні контейнери з кришками, джерело спрямованого світла (наприклад, лазерна указка), кухонна сіль, розчин ПАР (наприклад, рідкий миючий засіб), 1 куряче яйце, розведений розчин соляної кислоти.
Проведення експерименту:
Наливаємо воду в скляний контейнер, повністю розчиняємо у ньому трохи кухонної солі.
Висвітлюємо збоку склянку з отриманим розчином вузьким променем світла (промінь лазерної указки). Оскільки сіль повністю розчинилася, жодного помітного ефекту немає.
Експеримент із біологічним матеріалом:
Розчиняємо курячий білок приблизно 300мл 1% розчину солі.
Висвітлюємо отриманий розчин вузьким променем світла. Якщо подивитися на склянку збоку, на шляху променя видно яскрава смуга, що світиться - поява ефекту Тіндаля.
Потім додаємо в розчин білка розведений розчин соляної кислоти. Білок згорнеться (денатурує) з утворенням білястого осаду. У верхній частині склянки промінь світла знову не буде видно.
Результати експерименту:Якщо спрямувати промінь світла збоку на скляну склянку з розчином солі, промінь буде невидимий у розчині. Якщо промінь світла пропустити через склянку з колоїдним розчином (розчин ПАР), він буде видно, тому що відбувається розсіювання світла на колоїдних частинках.
Вплив довжини хвилі, розміру частинок та концентрації на реалізацію ефекту Тіндаля
Довжина хвилі.Оскільки найкоротшу довжину з видимого спектру мають хвилі кольорів синьої гами, саме ці хвилі відбиваються від частинок при ефекті Тіндаля, а довгі червоні розсіюються гірше.
Розмір частинок.Якщо збільшується розмір частинок, то вони можуть впливати на розсіювання світла будь-якої довжини хвилі, і «розщеплена» веселка складається назад, отримуючи повністю біле світло.
Концентрація частинок.Інтенсивність розсіяного світла прямо пропорційна концентрації частинок колоїдному розчині.
Застосування ефекту Тіндаля
Засновані на ефекті Тіндаля методи виявлення, визначення розміру і концентрації колоїдних частинок широко застосовуються в наукових дослідженнях і промисловій практиці (наприклад, в ультрамікроскопах).
Ультрамікроскоп - оптичний прилад для виявлення дрібних (колоїдних) частинок, розміри яких менші за межу дозволу звичайних світлових мікроскопів. Можливість виявлення таких частинок з допомогою ультрамікроскопа обумовлена дифракцією світла ними ефектом Тиндаля. При сильному бічному освітленні кожна частка в ультрамікроскопі відзначається спостерігачем як яскрава точка (дифракційна пляма, що світиться) на темному тлі. Внаслідок дифракції на найдрібніших частинках дуже мало світла, тому в ультрамікроскопі застосовують, як правило, сильні джерела світла.
Залежно від інтенсивності освітлення, довжини світлової хвилі, різниці показників заломлення частки та середовища можна виявити частинки розмірами від 20-50 нм до 1-5 мкм. За дифракційними плямами не можна визначити справжні розміри, форму та структуру частинок. Ультрамікроскоп не дає оптичних зображень досліджуваних об'єктів. Однак, використовуючи ультрамікроскоп, можна встановити наявність і чисельну концентрацію частинок, вивчити їх рух, а також розрахувати середній розмір частинок, якщо відомі їх вагова концентрація і щільність.
Ультрамікроскопи застосовують для дослідження дисперсних систем, контролю чистоти атмосферного повітря. Води, ступеня забруднення оптично прозорих середовищ сторонніми включеннями.
Висновок
У процесі свого дослідження я багато дізналася про оптичні ефекти, зокрема, про ефект Тіндаля. Ця робота допомогла мені по-новому подивитись як деякі розділи фізики, і наш дивовижний світ загалом.
Крім аспектів, розглянутих у цій роботі, на мою думку, було б цікаво вивчити можливості більш широкого практичного застосування ефекту Тіндаля.
Що ж стосується призначення дослідження, то воно може бути корисним і цікавим учням шкіл, які захоплюються оптикою, а також усім, хто цікавиться фізикою та різноманітними експериментами.
Список літератури
Гавронська Ю.Ю. Колоїдна хімія: Підручник. СПб.: Вид-во РДПУ ім. А. І. Герцена, 2007. – 267 с.
Новий політехнічний словник. - М.: Велика Російська енциклопедія, 2000. - .20 с. , 231 с. , 460 с.
Посібник із виконання експериментів до «NanoSchoolBox». NanoBioNet e.V/ Scince Park Переклад ІНТ.
https://indicator.ru/article/2016/12/04/istoriya-nauki-chelovek-rasseyanie.
http://kf.info.urfu.ru/fileadmin/user_upload/site_62_6389/pdf/FiHNS_proceedings.pdf
http://www.ngpedia.ru/id623274p1.html
ЕЛЕКТРОКІНЕТИЧНІ ВЛАСТИВОСТІ КОЛОЇДІВ
Електрокінетичні явища поділяють на дві групи: прямі та зворотні. До прямих відносять електрокінетичні явища, які виникають під дією зовнішнього електричного поля (електрофорез і електроосмос). Зворотними називають електрокінетичні явища, у яких при механічному переміщенні однієї фази щодо іншої виникає електричний потенціал (потенціал перебігу та потенціал седиментації).
Електрофорез та електроосмос були відкриті Ф. Рейссом (1808). Він виявив, що якщо у вологу глину занурити дві скляні трубки, заповнити їх водою та помістити в них електроди, то при пропусканні постійного струму відбувається рух частинок глини до одного з електродів.
Це явище переміщення частинок дисперсної фази постійному електричному полі було названо електрофорезом.
В іншому досвіді середня частина U-подібної трубки, що містить воду, була заповнена товченим кварцом, кожне коліно трубки поміщений електрод і пропущений постійний струм. Через деякий час у коліні, де знаходився негативний електрод, спостерігалося підвищення рівня води, в іншому - опускання. Після вимкнення електричного струму рівні води в колінах трубки вирівнювалися.
Це переміщення дисперсійної середовища щодо нерухомої дисперсної фази в постійному електричному полі названо электроосмосом.
Пізніше Квінке (1859) виявив явище, обернене до електроосмосу, назване потенціалом протікання. Воно полягає в тому, що при перебігу рідини під тиском через пористу діафрагму виникає різниця потенціалів. Як матеріал діафрагм були випробувані глина, пісок, дерево, графіт.
Явище, зворотне електрофорезу, і назване потенціалом седиментації, було відкрито Дорном (1878). При осіданні частинок суспензії кварцу під дією сили тяжіння виникала різниця потенціалів між рівнями різної висоти судини.
Всі електрокінетичні явища ґрунтуються на наявності подвійного електричного шару на межі твердої та рідкої фаз.
http://junk.wen.ru/o_6de5f3db9bd506fc.html
18. Особливі оптичні властивості колоїдних розчинів обумовлені їх головними особливостями: дисперсністю та гетерогенністю. На оптичні властивості дисперсних систем значною мірою впливають розмір та форма частинок. Проходження світла через колоїдний розчин супроводжується такими явищами, як поглинання, відбиття, заломлення та розсіювання світла. Переважання якогось із цих явищ визначається співвідношенням між розміром частинок дисперсної фази і довжиною хвилі падаючого світла. У грубодисперсних системахв основному спостерігається відбиток світла поверхні частинок. У колоїдних розчинахрозміри частинок можна порівняти з довжиною хвилі видимого світла, що зумовлює розсіювання світла рахунок дифракції світлових хвиль.
Світлорозсіювання в колоїдних розчинах проявляється у вигляді опалесценції- матового свічення (зазвичай блакитних відтінків), яке добре помітне на темному тлі при бічному освітленні золю. Причиною опалесценції є розсіювання світла на колоїдних частинках рахунок дифракції. З опалесценцією пов'язане характерне для колоїдних систем явище - ефект Тіндаля: при пропусканні пучка світла через колоїдний розчин з напрямків, перпендикулярних до променя, спостерігається утворення в розчині конуса, що світиться.
Ефект Тіндаля, розсіювання Тіндаля - оптичний ефект, розсіювання світла під час проходження світлового пучка через оптично неоднорідне середовище. Зазвичай спостерігається у вигляді конуса (конус Тиндаля), що світиться, видимого на темному тлі.
Характерний для розчинів колоїдних систем (наприклад, золей металів, розбавлених латексів, тютюнового диму), в яких частинки та навколишнє середовище розрізняються за показником заломлення. На ефекті Тіндаля заснований ряд оптичних методів визначення розмірів, форми та концентрації колоїдних частинок та макромолекул. .
19. Золі -це малорозчинні речовини (солі кальцію, магнію, холестерину та ін) існуючі у вигляді ліофобних колоїдних розчинів.
Ньютонівська рідина - в'язка рідина, що підпорядковується у своїй течії закону в'язкого тертя Ньютона, тобто дотична напруга і градієнт швидкості в такій рідині лінійно залежні. Коефіцієнт пропорційності між цими величинами відомий як в'язкість.
Ньютонівська рідина продовжує текти, навіть якщо зовнішні сили дуже малі, аби вони не були строго нульовими. Для ньютонівської рідини в'язкість, за визначенням, залежить лише від температури та тиску (а також від хімічного складу, якщо рідина не є безпримесною), і не залежить від сил, що діють на неї. Типова ньютонівська рідина – вода.
Неньютонівською рідиною називають рідину, при перебігу якої її в'язкість залежить від градієнта швидкості. Зазвичай такі рідини дуже неоднорідні і складаються з великих молекул, що утворюють складні просторові структури.
Найпростішим наочним побутовим прикладом може бути суміш крохмалю з невеликою кількістю води. Чим швидше відбувається зовнішній вплив на зважені в рідині макромолекули сполучної речовини, тим вища її в'язкість.
***На Ньютона впало яблуко, китайці милувалися краплями на квітках лотоса, а Джон Тіндаль, мабуть, гуляючи лісом, помітив конус світла. Казка? Можливо. Але саме на честь останнього героя названо один із найпрекрасніших ефектів нашого світу – ефект Тіндаля...***
Розсіювання світла є однією із загальних характеристик високодисперсних систем.
При бічному освітленні дисперсної системи спостерігається характерне переливчасте, як правило, блакитне свічення, особливо добре видно на темному тлі.
Це властиво, пов'язане з розсіюванням світла частинками дисперсної фази, називають опалесценцією, від назви опала - opalus (лат.), напівпрозорого мінералу блакитно-або жовтувато-білого кольору. У 1868 році виявив, що при освітленні колоїдного розчину збоку пучком світла від сильного джерела спостерігається яскравий конус, що рівномірно світиться. конус Тіндаля,або ефект Тіндаля, тоді як разі низькомолекулярного розчину рідина здається оптично порожній, тобто. слід променя невидимий.
ліворуч - 1% розчин крохмалю, праворуч - вода.
Ефект Тіндаля виникає при розсіянні на завислих частках, розміри яких перевищують розміри атомів у десятки разів. При укрупненні частинок суспензії до розмірів порядку 1/20 довжини світлових хвиль (приблизно від 25 нм і вище) розсіювання стає поліхромним, тобто світло починає розсіюватися рівномірно у всьому видимому діапазоні кольорів від фіолетового до червоного. В результаті ефект Тіндаля зникає. Ось чому густий туман або купові хмари здаються нам білими - вони складаються з щільної суспензії водяного пилу з діаметром частинок від мікронів до міліметрів, що значно вище за поріг розсіювання по Тиндалю.
Можна подумати, що небо здається нам синьо-блакитним завдяки ефекту Тіндаля, але це не так. У відсутність хмарності або задимлення небо забарвлюється в синьо-блакитний колір завдяки розсіянню «денного світла» на молекулах повітря. Такий тип розсіювання називається розсіюванням Релея (на честь сера Релея). При розсіянні Релея синє і блакитне світло розсіюється навіть сильніше, ніж при ефекті Тіндаля: наприклад, синє світло з довжиною хвилі 400 нм розсіюється в чистому повітрі в дев'ять разів сильніше за червоне світло з довжиною хвилі 700 нм. Ось чому небо здається нам синім – сонячне світло розсіюється у всьому спектральному діапазоні, але в синій частині спектру майже на порядок сильніше, ніж у червоній. Ще сильніше розсіюються ультрафіолетові промені, що обумовлюють сонячну засмагу. Саме тому засмага розподіляється по тілу досить рівномірно, охоплюючи навіть ті ділянки шкіри, на які не потрапляють прямі сонячні промені.
Герасименко Євгенія
Дана презентація присвячена опису Ефекту Тіндаля та його практичного застосування.
Завантажити:
Попередній перегляд:
Щоб скористатися попереднім переглядом презентацій, створіть собі обліковий запис Google і увійдіть до нього: https://accounts.google.com
Підписи до слайдів:
Виконала: учениця 11 класу "Б" Герасименко Євгенія Перевірила: вчитель хімії Юркіна Т.І. 2012/2013 навчальний рік ефект тиндалю
Джон ТІНДАЛЬ Ірландський фізик та інженер. Народився Лайлін-Брідж, графство Карлоу. Після закінчення середньої школи працював топографом-геодезистом у військових організаціях та на будівництві залізниць. Одночасно закінчив механічний інститут у Престоні. Звільнений із військово-геодезичної служби за протести проти поганих умов праці. Викладав у Куінвуд-коледжі (Хемпшир), одночасно продовжував самоосвіту. У 1848-51 рр. слухав лекції у Марбурзькому та Берлінському університетах. Повернувшись до Англії, став викладачем, а згодом і професором Королівського інституту в Лондоні. Основні праці вченого присвячені магнетизму, акустиці, поглинанню теплового випромінювання газами та парами, розсіянню світла у каламутних середовищах. Вивчав будову та рух льодовиків в Альпах. Тиндаль був вкрай захоплений ідеєю популяризації науки. Регулярно читав публічні лекції, часто у формі безкоштовних лекцій всім бажаючих: для робітників на заводських дворах в обідні перерви, різдвяні лекції для дітей у Королівському інституті. Слава Тіндаля як популяризатора досягла й іншого берега Атлантики – весь тираж американського видання його книги «Фрагменти науки» було розкуплено за один день. Загинув у 1893 році безглуздою смертю: готуючи обід, дружина вченого (що пережила його на 47 років) помилково використовувала замість кухонної солі один із хімічних реактивів, що зберігалися на кухні.
Опис Тиндаля ефект - світіння оптично неоднорідного середовища внаслідок розсіювання світла, що проходить через неї. Зумовлений дифракцією світла на окремих частинках або елементах структурної неоднорідності середовища, розмір яких набагато менше довжини хвилі світла, що розсіюється. Характерний для колоїдних систем (наприклад, гідрозолей, тютюнового диму) з низькою концентрацією частинок дисперсної фази, що мають показник заломлення, відмінний від показника заломлення дисперсійного середовища. Зазвичай спостерігається у вигляді світлого конуса на темному тлі (конус Тіндаля) при пропусканні сфокусованого світлового пучка збоку через скляну кювету з плоскопаралельними стінками, заповнену колоїдним розчином. Короткохвильова складова білого (немонохроматичного) світла розсіюється колоїдними частинками сильніше за довгохвильову, тому утворений ним конус Тіндаля в непоглинаючому золі має блакитний відтінок. Тіндаля ефект по суті те саме, що опалесценція. Але традиційно перший термін відносять до інтенсивного розсіювання світла в обмеженому просторі по ходу променя, а другий - до слабкого розсіювання світла всім обсягом об'єкта, що спостерігається.
Тиндаля ефект сприймається неозброєним оком як рівномірне світіння деякої частини об'єму системи, що розсіює світло. Світло походить від окремих точок - дифракційних плям, добре помітних під оптичним мікроскопом при досить сильному висвітленні розбавленого золю. Інтенсивність розсіяного в даному напрямку світла (при постійних параметрах падаючого світла) залежить від кількості частинок, що розсіюють, і їх розміру.
Часові характеристики Час ініціації (log to від -12 до -6); час існування (log tc від -12 до 15); Час деградації (log td від -12 до -6); Час оптимального прояву (log tk від -9 до -7). Технічна реалізація ефекту Ефект може легко спостерігатись при пропусканні пучка гелій-неонового лазера через колоїдний розчин (просто незабарвлений крохмальний кисіль). Діаграма
Застосування ефекту Засновані на ефекті Тіндаля методи виявлення, визначення розміру і концентрації колоїдних частинок (ультрамікроскопія, нефелометрія широко застосовуються в наукових дослідженнях і промисловій практиці).
приклад. Ультрамікроскоп. Ультрамікроскоп - оптичний прилад для виявлення дрібних (колоїдних) частинок, розміри яких менші за межу дозволу звичайних світлових мікроскопів. Можливість виявлення таких частинок за допомогою ультрамікроскопа обумовлена дифракцією світла на них ефектом Тиндаля. При сильному бічному освітленні кожна частка в ультрамікроскопі відзначається спостерігачем як яскрава точка (дифракційна пляма, що світиться) на темному тлі. Внаслідок дифракції на найдрібніших частинках дуже мало світла, тому в ультрамікроскопі застосовують, як правило, сильні джерела світла. Залежно від інтенсивності освітлення, довжини світлової хвилі, різниці показників заломлення частки та середовища можна виявити частинки розмірами від 20-50 нм до 1-5 мкм. За дифракційними плямами не можна визначити справжні розміри, форму та структуру частинок. Ультрамікроскоп не дає оптичних зображень досліджуваних об'єктів. Однак, використовуючи ультрамікроскоп, можна встановити наявність і чисельну концентрацію частинок, вивчити їх рух, а також розрахувати середній розмір частинок, якщо відомі їх вагова концентрація і щільність. У схемі щілинного ультрамікроскопа (рис. 1а) система, що досліджується, нерухома.
У схемі щілинного ультрамікроскопа система, що досліджується, нерухома. Принципова схема щілинного мікроскопа. Кювета 5 з об'єктом, що досліджується, висвітлюється джерелом світла 1 (2 - конденсатор, 4 - освітлювальний об'єктив) через вузьку прямокутну щілину 3, зображення якої проектується в зону спостереження. В окуляр спостережного мікроскопа 6 видно крапки частинок, що світяться, що знаходяться в площині зображення щілини. Вище та нижче освітленої зони присутність частинок не виявляється.
У потоковому ультрамікроскопі частинки, що вивчаються, рухаються по трубці назустріч оку спостерігача. Принципова схема потокового мікроскопа Перетинаючи зону освітлення вони реєструються як яскраві спалахи візуально або за допомогою фотометричного пристрою. Регулюючи яскравість освітлення спостерігаються частинок рухомим фотометричним клином 7, можна виділяти для реєстрації частинки, розмір яких перевищує задану межу. За допомогою сучасного потокового ультрамікроскопа з лазерним джерелом світла та оптико-електронною системою реєстрації частинок визначають концентрацію частинок в аерозолях в межах від 1 до 109 частинок в 1 см3, а також знаходять функції розподілу частинок за розмірами. Ультрамікроскопи застосовують для дослідження дисперсних систем, контролю чистоти атмосферного повітря. Води, ступеня забруднення оптично прозорих середовищ сторонніми включеннями.
Використовувана литература 1. Фізика. Великий енциклопедичний словник. - М.: Велика Російська енциклопедія, 1999. - С.90, 460. 2. Новий політехнічний словник. - М.: Велика Російська енциклопедія, 2000. - С.20, 231, 460. неоднорідне двофазне середовище розсіювання світла дисперсне середовище
За оптичними властивостями колоїдні розчини істотно відрізняються від істинних розчинів низькомолекулярних речовин, а також від грубодисперсних систем. Найбільш характерними оптичними властивостями колоїдно-дисперсних систем є опалесценція, ефект Фарадея – Тіндаля та забарвлення. Всі ці явища обумовлені розсіюванням та поглинанням світла колоїдними частинками.
Залежно від довжини хвилі видимого світла та відносних розмірів частинок дисперсної фази розсіювання світла набуває різного характеру. Якщо розмір частинок перевищує довжину світлових хвиль, світло від них відбивається за законами геометричної оптики. При цьому частина світлового випромінювання може проникати всередину частинок, зазнавати заломлення, внутрішнє відображення та поглинатися.
Якщо розмір частинок менший за довжину напівхвилі падаючого світла, спостерігається дифракційне розсіювання світла; світло хіба що обходить (огинає) часточки, що зустрічаються на шляху. При цьому має місце часткове розсіювання у вигляді хвиль, що розходяться на всі боки. Через війну розсіяння світла кожна частка є джерелом нових, менш інтенсивних хвиль, т. е. відбувається хіба що самосвічення кожної частки. Явище розсіяння світла найдрібнішими частинками отримало назву опалесценції.Воно властиве переважно золям (рідким і твердим), спостерігається лише у відбитому світлі, тобто збоку чи темному тлі. Виражається це явище у появі деякої каламутності золю і в зміні («переливах») його забарвлення в порівнянні з забарвленням у світлі, що проходить. Забарвлення у відбитому світлі, зазвичай, зсунуто у бік більшої частоти видимої частини спектра. Так, білі золі (золь хлориду срібла, каніфолі та ін) опалескують блакитним кольором.
Ефект Фарадея – Тіндаля.Дифракційне розсіювання світла вперше було помічено М. В. Ломоносовим. Пізніше, 1857 р., це явище спостерігав Фарадей у золях золота. Найбільш детально явище дифракції (опалесценції) для рідких та газових середовищ було вивчено Тіндалем (1868).
Якщо взяти одну склянку з розчином хлориду натрію, а інший - з гідрозолем яєчного білка, важко встановити, де колоїдний розчин, а де істинний, оскільки на вигляд обидві рідини безбарвні та прозорі (рис. 6.5). Однак ці розчини можна легко розрізнити, зробивши наступний досвід. Надягнемо на джерело світла (настільну лампу) світлонепроникний футляр з отвором, перед яким з метою отримання більш вузького і яскравого пучка світла поставимо лінзу. Якщо на шляху променя світла поставити обидві склянки, у склянці із золем побачимо світлову доріжку (конус), тоді як у склянці з хлоридом натрію промінь майже непомітний. На ім'я вчених, які вперше спостерігали це явище, конус, що світиться, в рідині був названий конусом (або ефектом) Фарадея - Тиндаля. Цей ефект характерний для всіх колоїдних розчинів.
Поява конуса Фарадея – Тіндаля пояснюється явищем розсіювання світла колоїдними частинками розміром 0,1-0,001 мкм.
Довжина хвиль видимої частини спектру 0,76-0,38 мкм, тому кожна колоїдна частка розсіює світло, що падає на неї. Він видно в конусі Фарадея - Тіндаля, коли промінь зору спрямований під кутом до променя, що проходить через золь. Таким чином, ефект Фарадея - Тиндаля - явище, ідентичне опалесценції, і відрізняється від останньої лише видом колоїдного стану, тобто мікрогетерогенності системи.
Теорія розсіювання світла колоїдно-дисперсними системами була розроблена Релеєм в 1871 р. Вона встановлює залежність інтенсивності (кількості енергії) розсіяного світла (I) при опалесценції та в конусі Фарадея – Тіндаля від зовнішніх та внутрішніх факторів. Математично ця залежність виражається у вигляді формули, що отримала назву формули Релея:
| | 6.1 |
де I - інтенсивність розсіяного світла у напрямі, перпендикулярному до променя падаючого світла; К - константа, яка залежить від показників заломлення дисперсійного середовища та дисперсної фази; n – число частинок в одиниці об'єму золю; λ - довжина хвилі падаючого світла; V – обсяг кожної частинки.
З формули (6.1) випливає, що розсіювання світла (I) пропорційно концентрації частинок, квадрату об'єму частинки (або для сферичних частинок - шостого ступеня їхнього радіусу) і обернено пропорційно четвертого ступеня довжини хвилі падаючого світла. Отже, розсіювання коротких хвиль відбувається щодо інтенсивніше. Тому безбарвні золі в світлі, що проходить, здаються червонуватими, в розсіяному - блакитними.
Забарвлення колоїдних розчинів.В результаті вибіркового поглинання світла (абсорбції) у поєднанні з дифракцією утворюється те чи інше забарвлення колоїдного розчину. Досвід показує, що більшість колоїдних (особливо металевих) розчинів яскраво забарвлено в найрізноманітніші кольори, починаючи від білого і закінчуючи абсолютно чорним, з усіма відтінками спектру кольорів. Так, золі As 2 S 3 мають яскраво-жовтий, Sb 2 S 3 - помаранчевий, Fe(OH) 3 - червонувато-коричневий, золота - яскраво-червоний колір тощо.
Один і той же золь має різне забарвлення в залежності від того, у проходить або відбитому світлі вона розглядається. Золі однієї і тієї ж речовини в залежності від способу приготування можуть набувати різного забарвлення - явище поліхромії (багатоцвітості). Забарвлення золів у разі залежить від ступеня дисперсності частинок. Так, грубодисперсні золі золота мають синє забарвлення, більшою мірою дисперсності - фіолетове, а високодисперсні - яскраво - червоне. Цікаво відзначити, що колір металу в недисперсному стані немає нічого спільного з його кольором в колоїдному стані.
Необхідно відзначити, що інтенсивність фарбування золів у десятки (а то й у сотні) разів більша, ніж молекулярних розчинів. Так, жовте забарвлення золю As 2 S 3 в шарі товщиною 1 см добре помітна при масовій концентрації 10 -3 г/л, а червоний колір золю золота помітний навіть при концентрації 10 -5 г/л.
Красиве і яскраве забарвлення багатьох дорогоцінних і напівдорогоцінних каменів (рубінів, смарагдів, топазів, сапфірів) обумовлено вмістом у них нікчемних (не визначальних навіть на кращих аналітичних вагах) кількостей домішок важких металів та їх оксидів, що перебувають у колоїдному стані. Так, для штучного отримання яскравого рубінового скла, що вживається для автомобільних, велосипедних та інших ліхтарів, достатньо на 1000 кг скляної маси додати лише 0,1 кг колоїдного золота.