Скорость большинства химических реакций возрастает при повышении температуры. Так как концентрация реагирующих веществ, практически не зависит от температуры, то в соответствии с кинетическим уравнением реакции основное влияние температуры на скорость реакции осуществляется через изменение константы скорости реакции. При увеличении температуры возрастает энергия сталкивающихся частиц и повышается вероятность того, что при столкновении произойдет химическое превращение.
Зависимость скорости реакции от температуры можно характеризовать величиной температурного коэффициента .
Экспериментальные данные по влиянию температуры на скорость многих химических реакций при обычных температурах (273–373 К), в небольшом интервале температур показали, что повышение температуры на 10 градусов увеличивает скорость реакции в 2-4 раза (правило Вант-Гоффа).
По Вант-Гоффу- температурный коэффициент константы скорости (коэффициент Вант-Гоффа ) – это возрастание скорости реакции при увеличении температуры на 10 градусов.
![]() (4.63)
(4.63)
где и - константы скорости при температурах и ; - температурный коэффициент скорости реакции.
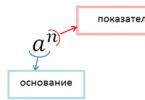
При повышении температуры на n десятков градусов отношение констант скоростей будет равно
где n может быть как целым, так и дробным числом.
Правило Вант-Гоффа это приближенное правило. Оно применимо в узком интервале температур, так как температурный коэффициент изменяется с температурой.
Более точная зависимость константы скорости реакции от температуры выражается полуэмпирическим уравнением Аррениуса
где А - предэкспоненциальный множитель который не зависит от температуры, а определяется только видом реакции; Е – энергия активации химической реакции. Энергию активации можно представить как некоторую пороговую энергию, характеризующую высоту энергетического барьера на пути реакции. Энергия активации также не зависит от температуры.
Эта зависимость установлена в конце XIX в. голландским ученым Аррениусом для элементарных химических реакций.
Энергия активации прямой (Е 1) и обратной (Е 2) реакции связана с тепловым эффектом реакции DН соотношением (см. рис 1):
Е 1 – Е 2 = DН.
Если реакция эндотермическая и DН> 0, то Е 1 > Е 2 и энергия активации прямой реакции больше обратной. Если реакция экзотермическая, то Е 1 < Е 2 .
Уравнение Аррениуса (101) в дифференциальной форме можно записать:
Из уравнения следует, что чем больше энергия активации Е, тем быстрее растет скорость реакции с температурой.
Разделив переменные k и T и, считая E постоянной величиной, после интегрирования уравнения (4.66) получим:

Рис. 5. График lnk –1/T .
![]() , (4.67)
, (4.67)
где А – предэкспоненциальный множитель, имеющий размерность константы скорости. Если это уравнение справедливо, то на графике в координатах опытные точки располагаются на прямой линии под углом a к оси абсцисс и угловой коэффициент () равен , что позволяет рассчитать энергию активации химической реакции по зависимости константы скорости от температуры по уравнению .
Энергию активации химической реакции можно вычислить по значениям констант скоростей при двух различных температурах по уравнению
![]() . (4.68)
. (4.68)
Теоретический вывод уравнения Аррениуса сделан для элементарных реакций. Но опыт показывает, что подавляющее большинство сложных реакций также подчиняются этому уравнению. Однако для сложных реакций энергия активации и предэкспоненциальный множитель в уравнении Аррениуса не имеют определенного физического смысла.
Уравнение Аррениуса (4.67) позволяет дать удовлетворительное описание большого круга реакций в узком температурном интервале.
Для описания зависимости скорости реакции от температуры применяют также модифицированное уравнение Аррениуса
![]() ,
(4.69)
,
(4.69)
в которое входят уже три параметра: А , Е и n .
Уравнение (4.69) широко используется для реакций, протекающих в растворах. Для некоторых реакций зависимость константы скорости реакции от температуры отличается от приведенных выше зависимостей. Так, например, в реакциях третьего порядка константа скорости убывает с увеличением температуры. В цепных экзотермических реакциях константа скорости реакции резко возрастает при температуре выше некоторого предела (тепловой взрыв).
4.5.1. Примеры решения задач
Пример 1. Константа скорости некоторой реакции с увеличением температуры изменялась следующим образом: t 1 = 20°С;
k 1 = 2,76 10 -4 мин. -1 ; t 2 = 50 0 С; k 2 = 137,4 10 -4 мин. -1 Определить температурный коэффициент константы скорости химической реакции.
Решение. Правило Вант –Гоффа позволяет рассчитать температурный коэффициент константы скорости по соотношению
g n = =2 ¸ 4, где n = = =3;
g 3 = =49,78 g = 3,68
Пример 2. С помощью правила Вант-Гоффа вычислить, при какой температуре реакция закончится за 15 мин., если при температуре 20 0 С потребовалось 120 мин. Температурный коэффициент скорости реакции равен 3.
Решение. Очевидно, чем меньше время протекания реакции (t ), тем больше константа скорости реакции:
3 n = 8, n ln3 = ln8, n= = .
Температура, при которой реакция закончится за 15 минут, равна:
20 + 1,9×10 = 39 0 С.
Пример 3. Константа скорости реакции омыления уксусно-этилового эфира раствором щелочи при температуре 282,4 К равна2,37л 2 /моль 2 мин. , а при температуре 287,40 К равна 3,2л 2 /моль 2 мин. Найти, при какой температуре константа скорости данной реакции равна 4?
Решение.
1. Зная значения констант скоростей при двух температурах, можно найти энергию активации реакции:
 =
= ![]() = 40,8 кДж/моль.
= 40,8 кДж/моль.
2. Зная значение энергии активации, из уравнения Аррениуса
Вопросы и задания для самоконтроля.
1.Какие величины называются «аррениусовскими» параметрами?
2.Какой минимум опытных данных необходим для расчета энергии активации химической реакции?
3. Покажите, что температурный коэффициент константы скорости зависит от температуры.
4. Существуют ли отклонения от уравнения Аррениуса? Как можно описать зависимость константы скорости от температуры в этом случае?
Кинетика сложных реакций
Реакции, как правило, не протекают путем непосредственного взаимодействия всех исходных частиц с прямым переходом их в продукты реакции, а состоят из нескольких элементарных стадий. Это, прежде всего, относится к реакциям, в которых, согласно их стехиометрическому уравнению, принимает участие более трех частиц. Однако, даже реакции двух или одной частицы часто идут не по простому би- или мономолекулярному механизму, а более сложным путем, то есть через ряд элементарных стадий.
Реакции называются сложными, если расходование исходных веществ и образование продуктов реакции происходит через ряд элементарных стадий, которые могут протекать одновременно или последовательно. При этом некоторые стадии проходят с участием веществ, не являющихся ни исходными веществами, ни продуктами реакции (промежуточные вещества).
В качестве примера сложной реакции можно рассмотреть реакцию хлорирования этилена с образованием дихлорэтана. Прямое взаимодействие и должно идти через четырехчленный активированный комплекс, что сопряжено с преодолением высокого энергетического барьера. Скорость такого процесса мала. Если же в системе тем или иным путем (например, при действии света) образуются атомы , то процесс может пойти по цепному механизму. Атом легко присоединяется по двойной связи с образованием свободного радикала - . Этот свободный радикал может легко оторвать атом от молекулы с образованием конечного продукта - , в результате чего регенерируется свободный атом .
В результате этих двух стадий одна молекула и одна молекула превращаются в молекулу продукта - , а регенерированный атом вступает во взаимодействие со следующей молекулой этилена. Обе стадии имеют невысокие энергии активации, и этот путь обеспечивает быстрое протекание реакции. С учетом возможности рекомбинации свободных атомов и свободных радикалов полная схема процесса может быть записана в виде:

При всем многообразии, сложные реакции можно свести к комбинации нескольких типов сложных реакций, а именно параллельных, последовательных и последовательно-параллельных реакций.
Две стадии называются последовательными , если частица, образующаяся в одной стадии, является исходной частицей в другой стадии. Например, в приведенной схеме последовательными являются первая и вторая стадии:
![]() .
.
Две стадии называются параллельными , если в обеих в качестве исходной принимают участие одни и те же частицы. Например, в схеме реакции параллельными являются четвертая и пятая стадии:
Две стадии называются последовательно-параллельными , если они являются параллельными по отношению к одной и последовательными по отношению к другой из участвующих в этих стадиях частиц.
Примером последовательно-параллельных стадий являются вторая и четвертая стадии данной схемы реакции.
К характерным признакам того, что реакция протекает по сложному механизму, относятся следующие признаки:
Несовпадение порядка реакции и стехиометрических коэффициентов;
Изменение состава продуктов в зависимости от температуры, начальных концентраций и других условий;
Ускорение или замедление процесса при добавлении в реакционную смесь небольших количеств веществ;
Влияние материала и размеров сосуда на скорость реакции и др.
При кинетическом анализе сложных реакций применяют принцип независимости: «Если в системе протекают одновременно несколько простых реакций, то основной постулат химической кинетики применяется к каждой из них, как если бы данная реакция была единственной». Этот принцип можно сформулировать и следующим образом: «Величина константы скорости элементарной реакции не зависит от того, протекают ли в данной системе одновременно другие элементарные реакции».
Принцип независимости справедлив для большинства реакций, протекающих по сложному механизму, но не является всеобщим, та как существуют реакции, в которых одни простые реакции влияют на протекание других (например, сопряженные реакции.)
Важное значение при изучении сложных химических реакций имеет принцип микрообратимости или детального равновесия :
если в сложном процессе устанавливается химическое равновесие, то скорости прямой и обратной реакции должны быть равны для каждой из элементарных стадий.
Наиболее распространенным случаем протекания сложной реакции будет случай, когда реакция идет через несколько простых стадий, протекающих с разными скоростями. Различие в скоростях приводит к тому, что кинетика получения продукта реакции может определяться закономерностями только одной реакции. Например, для параллельных реакций скорость всего процесса определяется скоростью наиболее быстрой стадии, а для последовательных – наиболее медленной. Следовательно, при анализе кинетики параллельных реакций при значительной разнице в константах можно пренебречь скоростью медленной стадии, а при анализе последовательных реакций – не обязательно определять скорость быстрой реакции.
В последовательных реакциях наиболее медленная реакция называется лимитирующей. У лимитирующей стадии самая маленькая константа скорости.
Если значения констант скоростей отдельных стадий сложной реакции близки, то необходим полный анализ всей кинетической схемы.
Введение понятия стадии, определяющей скорость, во многих случаях упрощает математическую сторону рассмотрения подобных систем и объясняет тот факт, что иногда кинетика сложных, многостадийных реакций хорошо описывается простыми уравнениями, например первого порядка.
Возрастание скорости реакции с ростом температуры принято характеризовать температурным коэффициентом скорости реакции, числом, показывающим, во сколько раз возрастает скорость данной реакции при повышении температуры системы на 10°С. Температурный коэффициент различных реакций различен. При обычных температурах его значение для большинства реакций находится в пределах от 2... 4.
Температурный коэффициент определяют в соответствии с так называемым «правилом Вант-Гоффа», которое математически выражается уравнением
v 2 /v 1 = g (T 2 – T 1)/10 ,
где v 1 и v 2 – скорости реакции при температурах Т 1 и Т 2 ; g - температурный коэффициент реакции.
Так, например, если g = 2, то при Т 2 – Т 1 = 50°С v 2 /v 1 = 2 5 = 32, т.е. реакция ускорилась в 32 раза, причем это ускорение никак не зависит от абсолютных величин Т 1 и Т 2 , а только от их разности.
Энергия активации, разность между значениями средней энергии частиц (молекул, радикалов, ионов и др.), вступающих в элементарный акт химической реакции, и средней энергии всех частиц, находящихся в реагирующей системе. Для различных химических реакций Э. а. изменяется в широких пределах - от нескольких до ~ 10 дж./ моль. Для одной и той же химической реакции значение Э. а. зависит от вида функций распределения молекул по энергиям их поступательного движения и внутренним степеням свободы (электронным, колебательным, вращательным). Как статистическую величину Э. а. следует отличать от пороговой энергии, или энергетического барьера, - минимальной энергии, которой должна обладать одна пара сталкивающихся частиц для протекания данной элементарной реакции.
Аррениуса уравнение , температурная зависимость константы скорости к элементарной хим. реакции:
где A-предэкспоненциальныи множитель (размерность совпадает с размерностью к), Е а -энергия активации, обычно принимающая положит. значения, Т-абс. температура, k-постоянная Больцмана. Принято приводить Е а в расчете не на одну молекулу. а на число частиц N A = 6,02*10 23 (постоянная Авогадро) и выражать в кДж/моль; в этих случаях в уравнении Аррениуса величину k заменяют газовой постоянной R. График зависимости 1nк от 1/kT (аррениусов график) – прямая линия, отрицательный наклон которой определяется энергией активации Е а и характеризует положит. температурную зависимость к.
Катализа́тор - химическое вещество, ускоряющее реакцию, но не входящее в состав продуктов реакции . Количество катализатора, в отличие от других реагентов, после реакции не изменяется. Важно понимать, что катализатор участвует в реакции. Обеспечивая более быстрый путь для реакции, катализатор реагирует с исходным веществом, получившееся промежуточное соединение подвергается превращениям и в конце расщепляется на продукт и катализатор. Затем катализатор снова реагирует с исходным веществом, и этот каталитический цикл многократно (до миллиона раз) [источник? ] повторяется.
Катализаторы подразделяются на гомогенные и гетерогенные . Гомогенный катализатор находится в одной фазе с реагирующими веществами, гетерогенный - образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества . Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al 2 O 3 , TiO 2 , ThO 2 , алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaO, BaO, MgO .
Гетерогенные катализаторы имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Для каждого типа реакций эффективны только определённые катализаторы. Кроме уже упомянутых кислотно-основных , существуют катализаторы окисления-восстановления ; для них характерно присутствие переходного металла или его соединения (Со +3 , V 2 O 5 +MoO 3). В этом случае катализ осуществляется путём изменения степени окисления переходного металла.
Диспе́рсная систе́ма - это образования из двух или более числа фаз (тел), которые совершенно или практически не смешиваются и не реагируют друг с другом химически. Первое из веществ (дисперсная фаза ) мелко распределено во втором (дисперсионная среда ). Если фаз несколько, их можно отделить друг от друга физическим способом (центрифугировать, сепарировать и т. д.).
Обычно дисперсные системы - это коллоидные растворы, золи. К дисперсным системам относят также случай твёрдой дисперсной среды, в которой находится дисперсная фаза.
Наиболее общая классификация дисперсных систем основана на различии в агрегатном состоянии дисперсионной среды и дисперсной фазы. Сочетания трех видов агрегатного состояния позволяют выделить девять видов дисперсных систем. Для краткости записи их принято обозначать дробью, числитель которой указывает на дисперсную фазу, а знаменатель на дисперсионную среду, например для системы «газ в жидкости» принято обозначение Г/Ж.
Коллоидные растворы. Коллоидное состояние характерно для многих веществ, если их частицы имеют размер от 1 до 500 нм. Легко показать, что суммарная поверхность этих частиц огромна. Если предположить, что частицы имеют форму шара с диаметром 10 нм, то при общем объеме этих частиц 1 см 3 они будут иметь
площадь поверхности порядка 10 м2. Как указывалось ранее поверхностный слой характеризуется поверхностной энергией и способностью адсорбировать те или иные частицы, в том числе ионы
из раствора. Характерной особенностью коллоидных частиц является наличие на их поверхности заряда, обусловленного избирательной адсорбцией ионов. Коллоидная частица имеет сложное строение. Она включает в себя ядро, адсорбированные ионы, противоины и растворитель. Существуют лиофильные (гид.
роф ильные) коллоиды, в которых растворитель взаимодейстиует с ядрами частиц, илнофобные (гидрофобные) коллоиды, в которых растворитель не взаимодействует с ядрами
частиц. Растворитель входит в состав гидрофобных частиц лишь как сольватная оболочка адсорбированных ионов или при наличии стабилизаторов (ПАВ), имеющих лиофобную и лиофильные части.
Приведем несколько примеров коллоидных частиц:
Как. видно, ядро состоит из электронейтрального агрегата частиц с адсорбированными ионами элементов, входящих в состав ядра (в данных примерах ионами Аg + , НS-, Fе 3+). Коллоидная час-шца кроме ядра имеет противоионы и молекулы растворителя. Адсорбированные ионы и противоионы с растворителем образуют адсорбированный слой. Суммарно заряд частицы равен разности зарядов адсороированных ионов и противоионов. Вокруг частиц находится д и ф ф у з н ы й с л о и и о н о в, заряд которых равен иряду коллоидной частицы. Коллоидная частица и диффузный слои образуют электронейтральную мицеллу
Мицеллы (уменьшительное от лат. mica - частица, крупинка) - частицы в коллоидных системах, состоят из нерастворимого в данной среде ядра очень малого размера, окруженного стабилизирующей оболочкой адсорбированных ионов и молекул растворителя. Например, мицелла сульфида мышьяка имеет строение:
{(As 2 S 3) m nHS − (n-x)H + } x- хН +
Средний размер мицелл от 10 −5 до 10 −7 см.
Коагуляция - разделение коллоидного раствора на две фазы – растворитель и студнеобразную массу, или загустевание раствора в результате укрупнения частиц растворенного вещества
Пептизация - процесс перехода коллоидного осадка или геля в коллоидный раствор под действием жидкости или добавленных к ней веществ, хорошо адсорбирующихся осадком или гелем, называемых в этом случае пептизаторами (например, пептизация жиров под действием желчи).
Пептизация - разъединение агрегатов частиц гелей (студней) или рыхлых осадков под влиянием определенных веществ - пептизаторов после коагуляции коллоидных растворов. В результате пептизации осадок (или гель) переходит во взвешенное состояние.
РАСТВОРЫ, однофазные системы, состоящие из двух или более компонентов. По своему агрегатному состоянию растворы могут быть твердыми, жидкими или газообразными.
Растворимость , способность вещества образовывать с другим веществом (или веществами) гомогенные смеси с дисперсным распределением компонентов (см. Растворы). Обычно растворителем считают вещество, которое в чистом виде существует в том же агрегатном состоянии, что и образовавшийся раствор. Если до растворения оба вещества находились в одном и том же агрегатном состоянии, растворителем считается вещество, присутствующее в смеси в существенно большем кол-ве.
Растворимость определяется физическим и химическим сродством молекул растворителя и растворяемого вещества, соотношением энергий взаимодействием однородных и разнородных компонентов раствора. Как правило, хорошо растворимы друг в друге подобные по физ. и хим. свойствам вещества (эмпирич. правило "подобное растворяется в подобном"). В частности, вещества, состоящие из полярных молекул, и вещества с ионным типом связи хорошо раств. в полярных растворителях (воде, этаноле, жидком аммиаке), а неполярные вещества хорошо раств. в неполярных растворителях (бензоле, сероуглероде).
Растворимость данного вещества зависит от температуры и давления соответствует общему принципу смещения равновесий (см. Ле Шателье-Брауна принцип). Концентрация насыщенного раствора при данных условиях численно определяет Р. вещества в данном растворителе и также наз. растворимостью. Пересыщенные растворы содержат большее кол-во растворенного вещества, чем это соответствует его растворимости, существование пересыщенных растворов обусловлено кинетич. затруднениями кристаллизации (см. Зарождение новой фазы). Для характеристики растворимости малорастворимых веществ используют произведение активностей ПА (для растворов, близких по своим свойствам к идеальному - произведение растворимости ПР).
Скорость хим.реакции возрастает с повышением температуры. Оценить возрастание скорости реакции с температурой можно воспользовавшись правилом Вант-Гоффа. Согласно правилу повышение температуры на 10 градусов увеличивает константу скорости реакции в 2-4 раза:
Это правило не выполняется при высоких температурах, когда константа скорости с температурой почти не изменяется.
Правило Вант-Гоффа позволяет быстро определить срок годности ЛВ. Повышение температуры увеличивает скорость разложения препарата. Это сокращает время установления срока годности лекарства.
Метод заключается в том, что ЛВ выдерживают пи повешенной температуре Т определенное время tТ, находят количество разложившегося препарата m и пересчитывают на стандартную температуру хранения 298К. Считая процесс разложения ЛВ реакцией первого порядка, выражают скорость при выбранной температуре Т и Т =298К:
Считая массу разложившегося препарата одинаковой для стандартных и реальных условий хранения, скорости разложения можно выразить равенствами:
Принимая T=298+10n, где n = 1,2,3…,
Получают окончательное выражение для срока хранения ЛВ при стандартных условиях 298К:
Теория активных соударений. Энергия активации. Уравнение Аррениуса. Связь между скоростью реакции и энергии активации.
Теория активных соударений была сформулирована С. Аррениусом в 1889 году. В основе этой теории лежит представление о том, что для протекания химической реакции необходимо соударение между молекулами исходных веществ, а число соударений определяется интенсивностью теплового движения молекул, т.е. зависит от температуры. Но не каждое соударение молекул приводит к химическому превращению: к нему приводит лишь активное соударение.
Активные соударения – это соударения, которые происходят, например, между молекулами А и В с большим запасом энергии. Тот минимальный запас энергии, которым должны обладать молекулы исходных веществ для того, чтобы их соударение было активным, называется энергетическим барьером реакции.
Энергия активации - это избыток энергии, которую можно сообщить или передать одному моль вещества.
Энергия активации ощутимо влияет на значение константы скорости реакции и ее зависимости от температуры: чем больше Еа, тем меньше константа скорости и тем значительнее влияет на нее изменение температуры.
Константа скорости реакции связана с энергией активации сложной зависимостью, описанной уравнением Аррениуса:
k=Aе–Ea/RT , где А – предэкспоненциальный множитель; Еа – энергия активации, R – универсальная газовая постоянная, равная 8,31 дж/моль; Т – абсолютная температура;
е-основание натуральных логарифмов.
Однако наблюдаемые константы скорости реакции, как правило, гораздо меньше, вычисленных по уравнению Аррениуса. Поэтому уравнение для константы скорости реакции видоизменяют следующим образом:
![]() (минус перед всей дробью)
(минус перед всей дробью)
Множитель приводит к тому, что температурная зависимость константы скорости отличается от уравнения Аррениуса. Поскольку энергия активации по Аррениусу рассчитывается как тангенс угла наклона логарифмической зависимости скорости реакции от обратной температуры, то проделав то же самое с уравнением ![]() , получим:
, получим:
Особенности гетерогенных реакций. Скорость гетерогенных реакций и факторы её определяющие. Кинетическая и диффузионная области гетерогенных процессов. Примеры гетерогенных реакций, представляющих интерес для фармации.
ГЕТЕРОГЕННЫЕ РЕАКЦИИ, хим. реакции с участием веществв, находящихся в разл. фазах и составляющих в совокупности гетерогенную систему. Типичные гетерогенные реакции: термич. разложение солей с образованием газообразных и твердых продуктов (напр., СаСО3 -> СаО + СО2), восстановление оксидов металлов водородом или углеродом (напр., РЬО + С -> Рb + СО), растворение металлов в кислотах (напр., Zn + + H2SO4 -> ZnSO4 + Н2), взаимод. твердых реагентов (А12О3 + NiO -> NiAl2O4). В особый класс выделяют гетерогенно-каталитические реакции, протекающие на поверхности катализатора; при этом реагенты и продукты могут и не находиться в разных фазах. Направление, при реакции N2 + + ЗН2 -> 2NH3, протекающей на поверхности железного катализатора, реагенты и продукт реакции находятся в газовой фазе и образуют гомогенную систему.
Особенности гетерогенных реакций обусловлены участием в них конденсированных фаз. Это затрудняет перемешивание и транспорт реагентов и продуктов; возможна активация молекул реагентов на поверхности раздела фаз. Кинетика любой гетерогенной реакции определяется как скоростью самого хим. превращения, так и процессами переноса (диффузией), необходимыми для восполнения расхода реагирующих веществ и удаления из реакционной зоны продуктов реакции. В отсутствие диффузионных затруднений скорость гетерогенной реакции пропорциональна размерам реакционной зоны; так называется удельная скорость реакции, рассчитанная на единицу поверхности (или объема) реакц. зоны, не изменяется во времени; для простых (одностадийных) реакций она м.б. определена на основе действующих масс закона. Этот закон не выполняется, если диффузия веществ протекает медленнее, чем хим. р-ция; в этом случае наблюдаемая скорость гетерогенной реакции описывается уравнениями диффузионной кинетики.
Скоростью гетерогенной реакции называется количество вещества, вступающего в реакцию или образующегося при реакции за единицу времени на единице площади поверхности фазы.
Факторы, влияющие на скорость химической реакции:
Природа реагирующих веществ,
Концентрация реагентов,
Температура,
Наличие катализатора.
Vгетерог= Δп(S Δt), где Vгетерог - скорость реакции в гетерогенной системе; п - число молей какого-либо из получающихся при реакции веществ; V - объем системы; t - время; S - площадь поверхности фазы, на которой протекает реакция; Δ - знак приращения (Δп = п2 - п1;Δt= t2- t1).
Задача 336.
При 150°С некоторая реакция заканчивается за 16 мин. Принимая температурный коэффициент скорости реакции равным 2,5, рассчитать, через какое время закончится эта реакция, если проводить ее: а) при 20
0
°С; б) при 80°С.
Решение:
Согласно правилу Вант Гоффа зависимость скорости от температуры выражается уравнением:
v t и k t - скорость и константа скорости реакции при температуре t°С; v (t + 10) и k (t + 10) те же величины при температуре (t + 10 0 C); - температурный коэффициент скорости реакции, значение которого для большинства реакций лежит в пределах 2 – 4.
а) Учитывая, что скорость химической реакции при данной температуре обратно пропорциональна продолжительности её протекания, подставим данные, приведённые в условии задачи в формулу, количественно выражающую правило Вант-Гоффа, получим:

б) Так как данная реакция протекает с понижением температуры, то при данной температуре скорость этой реакции прямо пропорциональна продолжительности её протекания, подставим данные, приведённые в условии задачи в формулу, количественно выражающую правило Вант-Гоффа, получим:

Ответ : а) при 200 0 С t2 = 9,8 c; б) при 80 0 С t3 = 162 ч 1мин 16 c.
Задача 337.
Изменится ли значение константы скорости реакции: а) при замене одного катализатора другим; б) при изменении концентраций реагирующих веществ?
Решение:
Константа скорости реакции – это величина, зависящая от природы реагирующих веществ, от температуры и от присутствия катализаторов, не зависит от концентрации реагирующих веществ. Она может быть равна скорости реакции в случае, когда концентрации реагирующих веществ равны единице (1 моль/л).
а) При замене одного катализатора другим изменится скорость данной химической реакции, она или увеличится. В случае применения катализатора увеличится скорость химической реакции, то, соответственно увеличится и значение константы скорости реакции. Изменение значения константы скорости реакции произойдёт и при замене одного катализатора другим, который увеличит или уменьшит скорость данной реакции по отношению к исходному катализатору.
б) При изменении концентрации реагирующих веществ изменится значения скорости реакции, а значение константы скорости реакции не изменится.
Задача 338.
Зависит ли тепловой эффект реакции от ее энергии активации? Ответ обосновать.
Решение:
Тепловой эффект реакции зависит только от начального и конечного состояния системы и не зависит от промежуточных стадий процесса. Энергия активации – это избыточная энергия, которой должны обладать молекулы веществ, для того чтобы их столкновение могло привести к образованию нового вещества. Энергию активации можно изменить повышением или понижением температуры, соответственно понижая или увеличивая её. Катализаторы понижают энергию активации, а ингибиторы – понижают.
Таким образом, изменение энергии активации приводит к изменению скорости реакции, но не к изменению теплового эффекта реакции. Тепловой эффект реакции – величина постоянная и не зависит от изменения энергии активации для данной реакции. Например, реакция образования аммиака из азота и водорода имеет вид:
Данная реакция экзотермическая, > 0). Реакция протекает с уменьшением числа молей реагирующих частиц и числа молей газообразных веществ, что приводит систему из менее устойчивого состояния в более устойчивое, энтропия уменьшается, < 0. Данная реакция в обычных условиях не протекает (она возможна только при достаточно низких температурах). В присутствии катализатора энергия активации уменьшается, и скорость реакции возрастает. Но, как до применения катализатора, так и в присутствии его тепловой эффект реакции не изменяется, реакция имеет вид:
Задача 339.
Для какой реакции прямой или обратной - энергия активации больше, если прямая реакция идет с выделением теплоты?
Решение:
Разность энергий активации прямой и обратной реакций равна тепловому эффекту: H = E a(пр.) - Е а(обр.) . Данная реакция протекает с выделением теплоты, т.е. является экзотермической, < 0 Исходя из этого, энергия активации прямой реакции имеет меньшее значение, чем энергия активации обратной реакции:
E a(пр.) < Е а(обр.) .
Ответ: E a(пр.) < Е а(обр.) .
Задача 340.
Во сколько раз увеличится скорость реакции, протекающей при 298 К, если энергию активации её уменьшить на 4 кДж/моль?
Решение:
Обозначим уменьшение энергии активации через Ea, а константы скоростей реакции до и после уменьшения энергии активации соответственно через k и k". Используя уравнение Аррениуса, получим:

E a - энергия активации, k и k" - константы скорости реакции, Т – температура в К (298).
Подставляя в последнее уравнение данные задачи и, выражая энергию активации в джоулях, рассчитаем увеличение скорости реакции:
![]()
Ответ : В 5 раз.
Скорость химической реакции зависит от температуры, причем при повышении температуры скорость реакции увеличивается. Голландский уч1ный Вант-Гофф показал, что при повышении температуры на 10 градусов скорость большинства реакций увеличивается в 2-4 раза;
VT 2 =VT 1 *y (T2-T1)/10
Где VT 2 и VT 1 – скорости реакции при температурах T 2 и T 1 ; у – температурный коэффициент скорости реакции, который показывает, во сколько раз увеличилась скорость реакции при повышении температуры на 10К.
При концентрации реагирующих веществ 1 моль/л скорость реакции численно равна константе скорости k. Тогда уравнение показывает, что константа скорости зависит от температуры так же, как и скорость процесса.
3. Напишите вариант реакции отщепления (элиминирования) с выделением галогенводорода .
C 2 H 5 Cl=C 2 H 4 +HCl
Билет №4
1. Что такое «атомная масса», «молекулярная масса», «моль вещества» и что принято за атомную единицу массы (а.е.м.)?
АТОМНАЯ МАССА - масса атома в атомных единицах массы (а. е. м.). За единицу а. е. м. принята 1/12 массы изотопа углерод- 12.
а.е.м. = 1/12 m 12 6 С = 1, 66 * 10 -24
МОЛЕКУЛЯРНАЯ МАССА - молярная масса соединения, отнесенная к 1/12 молярной массы атома углерода-12.
МОЛЬ - количество вещества, содержащее столько же частиц или структурных единиц (атомов, ионов, молекул, радикалов, электронов, эквивалентов и др.), что и в 12 а. е. м. изотопа углерода-12.
Формула увеличения скорости реакции в присутствии катализатора.
Изменить величину Еа (энергию активации) можно с помощью катализаторов. Вещества, принимающие участие, но не расходующиеся в процессе реакции, назваются катализаторами. Само это явление называется катализом. Увеличение скорости реакции в присутствии катализатора определяется формулой
В зависимости от того, находится ли катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. Механизм каталитического действия для них не одинков, однако и в том и в другом случае происходит ускорение реакции за счет снижения Еа. Существует ряд специфических катализаторов - ингибиторов, снижающих скорость реакции.
где -параметры каталитического процесса, V, k , Еа- некаталитического процесса.
Напишите реакции сгорания углеродсодержащих неорганических веществ в кислороде, указав окислитель и восстановитель, а также степени окисления углерода до и после реакции.
С – восстановитель, процесс окисления
О – окислитель, процесс восстановления
Билет № 5
1. Что такое «электроотрицательность», «валентность», «степень окисления» элемента и каковы основные правила их определения?
СТЕПЕНЬ ОКИСЛЕНИЯ - условный заряд атома элемента, полученный в предположении, что соединение состоит из ионов. Она может быть положительной, отрицательной, нулевой, дробной и обозначается арабской цифрой со знаком «+» или «-» в виде верхнего правого индекса символа элемента: С 1- , О 2- , Н + , Мg 2+ , N 3- , N 5+ , Сr 6+ .
Для определения степени окисления (с. о.) элемента в соединении (ионе) пользуются следующими правилами:
1 В простых веществах (Н2, S8, Р4) с. о. равна нулю.
2 Постоянную с. о. имеют щелочные (Э+) и щелочно-земельные (Э2+) элементы, а также фтор Р-.
3 Водород в большинстве соединений имеет с. о. Н+ (Н2О, СН4, НС1), в гидридах - Н- (-NaН, СаН2); с. о. кислорода, как правило, равна -2 (О2-), в пероксидах (-О-О-) - 1 (О-).
4 В бинарных соединениях неметаллов отрицательная с. о. приписывается элементу, расположенному справа).
5 Алгебраическая сумма с. о. молекулы равна нулю, иона - его заряду.
Способность атома присоединять или замещать определенное число других атомов называют ВАЛЕНТНОСТЬЮ. Мерой валентности считают число атомов водорода или кислорода, присоединенных к элементу, при условии, что водород одно- , а кислород двухвалентен.