Крайне редко химические вещества состоят из отдельных, не связанных между собой атомов химических элементов. Таким строением в обычных условиях обладает лишь небольшой ряд газов называемых благородными: гелий, неон, аргон, криптон, ксенон и радон. Чаще же всего химические вещества состоят не из разрозненных атомов, а из их объединений в различные группировки. Такие объединения атомов могут насчитывать несколько единиц, сотен, тысяч или даже больше атомов. Сила, которая удерживает эти атомы в составе таких группировок, называется химическая связь .
Другими словами, можно сказать, что химической связью называют взаимодействие, которое обеспечивает связь отдельных атомов в более сложные структуры (молекулы, ионы, радикалы, кристаллы и др.).
Причиной образования химической связи является то, что энергия более сложных структур меньше суммарной энергии отдельных, образующих ее атомов.
Так, в частности, если при взаимодействии атомов X и Y образуется молекула XY, это означает, что внутренняя энергия молекул этого вещества ниже, чем внутренняя энергия отдельных атомов, из которых оно образовалось:
E(XY) < E(X) + E(Y)
По этой причине при образовании химических связей между отдельными атомами выделятся энергия.
В образовании химических связей принимают участие электроны внешнего электронного слоя с наименьшей энергией связи с ядром, называемые валентными . Например, у бора таковыми являются электроны 2 энергетического уровня – 2 электрона на 2s- орбитали и 1 на 2p -орбитали:
При образовании химической связи каждый атом стремится получить электронную конфигурацию атомов благородных газов, т.е. чтобы в его внешнем электронном слое было 8 электронов (2 для элементов первого периода). Это явление получило название правила октета.
Достижение атомами электронной конфигурации благородного газа возможно, если изначально одиночные атомы сделают часть своих валентных электронов общими для других атомов. При этом образуются общие электронные пары.
В зависимости от степени обобществления электронов можно выделить ковалентную, ионную и металлическую связи.
Ковалентная связь
Ковалентная связь возникает чаще всего между атомами элементов неметаллов. Если атомы неметаллов, образующие ковалентную связь, относятся к разным химическим элементам, такую связь называют ковалентной полярной. Причина такого названия кроется в том, что атомы разных элементов имеют и различную способность притягивать к себе общую электронную пару. Очевидно, что это приводит к смещению общей электронной пары в сторону одного из атомов, в результате чего на нем формируется частичный отрицательный заряд. В свою очередь, на другом атоме формируется частичный положительный заряд. Например, в молекуле хлороводорода электронная пара смещена от атома водорода к атому хлора:
Примеры веществ с ковалентной полярной связью:
СCl 4 , H 2 S, CO 2 , NH 3 , SiO 2 и т.д.
Ковалентная неполярная связь образуется между атомами неметаллов одного химического элемента. Поскольку атомы идентичны, одинакова и их способность оттягивать на себя общие электроны. В связи с этим смещения электронной пары не наблюдается:
Вышеописанный механизм образования ковалентной связи, когда оба атома предоставляют электроны для образования общих электронных пар, называется обменным.
Также существует и донорно-акцепторный механизм.
При образовании ковалентной связи по донорно-акцепторному механизму общая электронная пара образуется за счет заполненной орбитали одного атома (с двумя электронами) и пустой орбитали другого атома. Атом, предоставляющий неподеленную электронную пару, называют донором, а атом со свободной орбиталью – акцептором. В качестве доноров электронных пар выступают атомы, имеющие спаренные электроны, например N, O, P, S.
Например, по донорно-акцепторному механизму происходит образование четвертой ковалентной связи N-H в катионе аммония NH 4 + :
Помимо полярности ковалентные связи также характеризуются энергией. Энергией связи называют минимальную энергию, необходимую для разрыва связи между атомами.
Энергия связи уменьшается с ростом радиусов связываемых атомов. Так, как мы знаем, атомные радиусы увеличиваются вниз по подгруппам, можно, например, сделать вывод о том, что прочность связи галоген-водород увеличивается в ряду:
HI < HBr < HCl < HF
Также энергия связи зависит от ее кратности – чем больше кратность связи, тем больше ее энергия. Под кратностью связи понимается количество общих электронных пар между двумя атомами.
Ионная связь
Ионную связь можно рассматривать как предельный случай ковалентной полярной связи. Если в ковалентной-полярной связи общая электронная пара смещена частично к одному из пары атомов, то в ионной она практически полностью «отдана» одному из атомов. Атом, отдавший электрон(ы), приобретает положительный заряд и становится катионом , а атом, забравший у него электроны, приобретает отрицательный заряд и становится анионом .
Таким образом, ионная связь — это связь, образованная за счет электростатического притяжения катионов к анионам.
Образование такого типа связи характерно при взаимодействии атомов типичных металлов и типичных неметаллов.
Например, фторид калия. Катион калия получается в результате отрыва от нейтрального атома одного электрона, а ион фтора образуется при присоединении к атому фтора одного электрона:

Между получившимися ионами возникает сила электростатического притяжения, в результате чего образуется ионное соединение.
При образовании химической связи электроны от атома натрия перешли к атому хлора и образовались противоположно заряженные ионы, которые имеют завершенный внешний энергетический уровень.
Установлено, что электроны от атома металла не отрываются полностью, а лишь смещаются в сторону атома хлора, как в ковалентной связи.
Большинство бинарных соединений, которые содержат атомы металлов, являются ионными. Например, оксиды, галогениды, сульфиды, нитриды.
Ионная связь возникает также между простыми катионами и простыми анионами (F − , Cl − , S 2-), а также между простыми катионами и сложными анионами (NO 3 − , SO 4 2- , PO 4 3- , OH −). Поэтому к ионным соединениям относят соли и основания (Na 2 SO 4 , Cu(NO 3) 2 , (NH 4) 2 SO 4), Ca(OH) 2 , NaOH).
Металлическая связь
Данный тип связи образуется в металлах.
У атомов всех металлов на внешнем электронном слое присутствуют электроны, имеющие низкую энергию связи с ядром атома. Для большинства металлов, энергетически выгодным является процесс потери внешних электронов.
Ввиду такого слабого взаимодействия с ядром эти электроны в металлах весьма подвижны и в каждом кристалле металла непрерывно происходит следующий процесс:
М 0 — ne − = M n + , где М 0 – нейтральный атом металла, а M n + катион этого же металла. На рисунке ниже представлена иллюстрация происходящих процессов.
То есть по кристаллу металла «носятся» электроны, отсоединяясь от одного атома металла, образуя из него катион, присоединяясь к другому катиону, образуя нейтральный атом. Такое явление получило название “электронный ветер”, а совокупность свободных электронов в кристалле атома неметалла назвали “электронный газ”. Подобный тип взаимодействия между атомами металлов назвали металлической связью.
Водородная связь
Если атом водорода в каком-либо веществе связан с элементом с высокой электроотрицательностью (азотом, кислородом или фтором), для такого вещества характерно такое явление, как водородная связь.
Поскольку атом водорода связан с электроотрицательным атомом, на атоме водорода образуется частичный положительный заряд, а на атоме электроотрицательного элемента — частичный отрицательный. В связи с этим становится возможным электростатическое притяжения между частично положительно заряженным атомом водорода одной молекулы и электроотрицательным атомом другой. Например водородная связь наблюдается для молекул воды:
Именно водородной связью объясняется аномально высокая температура плавления воды. Кроме воды, также прочные водородные связи образуются в таких веществах, как фтороводород, аммиак, кислородсодержащие кислоты, фенолы, спирты, амины.
Дипольные моменты молекул
Метод валентных связей основывается на положении, что каждая пара атомов в химической частице удерживается вместе при помощи одной или нескольких электронных пар. Эти пары электронов принадлежат двум связываемым атомам и локализованы в пространстве между ними. За счет притяжения ядер связываемых атомов к этим электронам и возникает химическая связь.
Перекрывание атомных орбиталей
При описании электронного строения химической частицы электроны, в том числе и обобществленные, относят к отдельным атомам и их состояния описывают атомными орбиталями. При решении уравнения Шредингера приближенную волновую функцию выбирают так, чтобы она давала минимальную электронную энергию системы, то есть наибольшее значение энергии связи. Это условие достигается при наибольшем перекрывании орбиталей, принадлежащей одной связи. Таким образом, пара электронов, связывающих два атома, находится в области перекрывания их атомных орбиталей.
Перекрываемые орбитали должны иметь одинаковую симметрию относительно межъядерной оси.
Перекрывание атомных орбиталей вдоль линии, связывающей ядра атомов, приводит к образованию σ-связей. Между двумя атомами в химической частице возможна только одна σ-связь. Все σ-связи обладают осевой симметрией относительно межъядерной оси. Фрагменты химических частиц могут вращаться вокруг межъядерной оси без нарушения степени перекрывания атомных орбиталей, образующих σ-связи. Совокупность направленных, строго ориентированных в пространстве σ-связей создает структуру химической частицы.
При дополнительном перекрывании атомных орбиталей, перпендикулярных линии связи, образуются π-связи.

В результате этого между атомами возникают кратные связи:
| Одинарная (σ) | Двойная (σ +π) | Тройная (σ + π + π) |
| F−F | O=O | N≡N |
С появлением π-связи, не имеющей осевой симметрии, свободное вращение фрагментов химической частицы вокруг σ-связи становится невозможным, так как оно должно привести к разрыву π-связи. Помимо σ- и π-связей, возможно образование еще одного вида связи - δ-связи:

Обычно такая связь образуется после образования атомами σ- и π-связей при наличии у атомов d
- и f
-орбиталей путем перекрывания их "лепестков" сразу в четырех местах. В результате кратность связи может возрасти до 4-5.
Например, в октахлородиренат(III)-ионе 2- между атомами рения образуются четыре связи.
Механизмы образования ковалентных связей
Различают несколько механизмов образования ковалентной связи: обменный (равноценный), донорно-акцепторный , дативный .
При использовании обменного механизма образование связи рассматривается как результат спаривания спинов свободных электронов атомов. При этом осуществляется перекрывание двух атомных орбиталей соседних атомов, каждая из которых занята одним электроном. Таким образом, каждый из связываемых атомов выделяет для обобществления пары по электрону, как бы обмениваясь ими. например, при образовании молекулы трифторида бора из атомов три атомные орбитали бора, на каждой из которых имеется по одному электрону, перекрываются с тремя атомными орбиталями трех атомов фтора (на каждой из них также находится по одному неспаренному электрону). В результате спаривания электронов в областях перекрывания соответствующих атомных орбиталей появляется три пары электронов, связывающих атомы в молекулу.
По донорно-акцепторному механизму перекрывается орбиталь с парой электронов одного атома и свободная орбиталь другого атома. В этом случае в области перекрывания также оказывается пара электронов. По донорно-акцепторному механизму происходит, например, присоединение фторид-иона к молекуле трифторида бора. Вакантная р -орбиталь бора (акцептора электронной пары) в молекуле BF 3 перекрывается с р -орбиталью иона F − , выступающего в роли донора электронной пары. В образовавшемся ионе − все четыре ковалентные связи бор−фтор равноценны по длине и энергии, несмотря на различие в механизме их образования.
Атомы, внешняя электронная оболочка которых состоит только из s - и р -орбиталей, могут быть либо донорами, либо акцепторами электронной пары. Атомы, у которых внешняя электронная оболочка включает d -орбитали, могут выступать в роли и донора, и акцептора пар электронов. В этом случае рассматривается дативный механизм образования связи. Примером проявления дативного механизма при образования связи служит взаимодействие двух атомов хлора. Два атома хлора в молекуле Cl 2 образуют ковалентную связь по обменному механизму, объединяя свои неспаренные 3р -электроны. Кроме того, происходит перекрывание 3р -орбитали атом Cl-1, на которой имеется пара электронов, и вакантной 3d -орбитали атома Cl-2, а также перекрывание 3р -орбитали атом Cl-2, на которой имеется пара электронов, и вакантной 3d -орбитали атома Cl-1. Действие дативного механизма приводит к увеличению прочности связи. Поэтому молекула Cl 2 является более прочной, чем молекула F 2 , в которой ковалентная связь образуются только по обменному механизму:
Гибридизация атомных орбиталей
При определении геометрической формы химической частицы следует учитывать, что пары внешних электронов центрального атома, в том числе и не образующие химическую связь, располагаются в пространстве как можно дальше друг от друга.
При рассмотрении ковалентных химических связей нередко используют понятие о гибридизации орбиталей центрального атома - выравнивание их энергии и формы. Гибридизация является формальным приемом, применяемым для квантово-химического описания перестройки орбиталей в химических частицах по сравнению со свободными атомами. Сущность гибридизации атомных орбиталей состоит в том, что электрон вблизи ядра связанного атома характеризуется не отдельной атомной орбиталью, а комбинацией атомных орбиталей с одинаковым главным квантовым числом. Такая комбинация называется гибридной (гибридизованной) орбиталью. Как правило, гибридизация затрагивает лишь высшие и близкие по энергии атомные орбитали, занятые электронами.
В результате гибридизации появляются новые гибридные орбитали (рис.24), которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары (или неспаренные электроны) оказались максимально удаленными друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. Поэтому тип гибридизации определяет геометрию молекулы или иона.
ТИПЫ ГИБРИДИЗАЦИИ
| Тип гибридизации | Геометрическая форма | Угол между связями | Примеры |
| sp | линейная | 180 o | BeCl 2 |
| sp 2 | треугольная | 120 o | BCl 3 |
| sp 3 | тетраэдрическая | 109,5 o | CH 4 |
| sp 3 d | тригонально-бипирамидальная | 90 o ; 120 o | PCl 5 |
| sp 3 d 2 | октаэдрическая | 90 o | SF 6 |
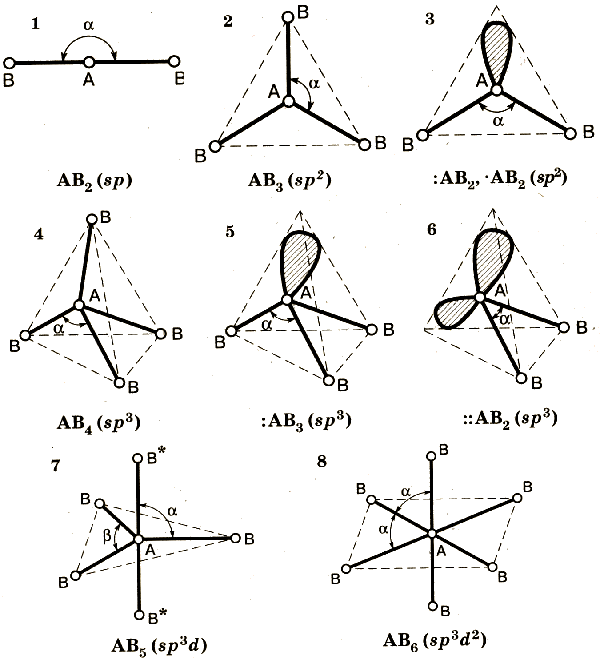
В гибридизации участвуют не только связывающие электроны, но и неподеленные электронные пары. Например, молекула воды содержит две ковалентные химические связи между атомом кислорода и двумя атомами водорода.

Помимо двух пар электронов, общих с атомами водорода, у атома кислорода имеются две пары внешних электронов, не участвующих в образовании связи (неподеленные электронные пары). Все четыре пары электронов занимают определенные области в пространстве вокруг атома кислорода.
Поскольку электроны отталкиваются друг от друга, электронные облака располагаются на возможно большем расстоянии друг от друга. При этом в результате гибридизации меняется форма атомных орбиталей, они вытянуты и направлены к вершинам тетраэдра. Поэтому молекула воды имеет угловую форму, а угол между связями кислород-водород равен 104,5 o .
Для предсказания типа гибридизации удобно использовать донорно-акцепторный механизм образования связи: происходит перекрывание пустых орбиталей менее электроотрицательного элемента и орбиталей более электроотрицательного элемента с находящимися на них парами электронов. При составлении электронных конфигураций атомов учитывают их степени окисления − условное число, характеризующее заряд атома в соединении, рассчитанный исходя из предположения ионного строения вещества.
Чтобы определить тип гибридизации и форму химической частицы, поступают следующим образом:
Наличие π-связей не влияет на тип гибридизации. Однако наличие дополнительного связывания может привести к изменению валентных углов, поскольку электроны кратных связей сильнее отталкиваются друг от друга. По этой причине, например, валентный угол в молекуле NO 2 (sp 2 -гибридизация) увеличивается от 120 o до 134 o .

Кратность связи азот−кислород в этой молекуле равна 1,5, где единица отвечает одной σ-связи, а 0,5 равно отношению числа орбиталей атома азота, не участвующих в гибридизации (1) к числу оставшихся активных электронных пар у атома кислорода, образующих π-связи (2). Таким образом, наблюдается делокализация π-связей (делокализованные связи − ковалентные связи, кратность которых не может быть выражена целым числом).
В случае sp , sp 2 , sp 3 , sp 3 d 2 гибридизации вершины в многограннике, описывающем геометрию химической частицы, равноценны, и поэтому кратные связи и неподеленные пары электронов могут занимать любые из них. Однако sp 3 d -гибридизации отвечает тригональная бипирамида , в которой валентные углы для атомов, расположенных в основании пирамиды (экваториальной плоскости), равны 120 o , а валентные углы с участием атомов, расположенных в вершинах бипирамиды, равны 90 o . Эксперимент показывает, что неподеленные электронные пары всегда располагаются в экваториальной плоскости тригональной бипирамиды. На этом основании делается вывод, что они требуют больше свободного пространства, чем пары электронов, участвующие в образовании связи. Примером частицы с таким расположением неподеленной электронной пары является тетрафторид серы (рис. 27). Если центральный атом одновременно имеет неподеленные пары электронов и образует кратные связи (например, в молекуле XeOF 2), то в случае sp 3 d -гибридизации именно они располагаются в экваториальной плоскости тригональной бипирамиды (рис. 28).
Дипольные моменты молекул
Идеальная ковалентная связь существует лишь в частицах, состоящих из одинаковых атомов (Н 2 , N 2 и т.д.). Если образуется связь между различными атомами, то электронная плотность смещается к одному из ядер атомов, то есть происходит поляризация связи. Характеристикой полярности связи служит ее дипольный момент.
Дипольный момент молекулы равен векторной сумме дипольных моментов ее химических связей (с учетом наличия неподеленных пар электронов). Если полярные связи расположены в молекуле симметрично, то положительные и отрицательные заряды компенсируют друг друга, и молекула в целом является неполярной. Так происходит, например, с молекулой диоксида углерода. Многоатомные молекулы с несимметричным расположением полярных связей (и, следовательно, электронной плотности) являются в целом полярными. Это относится, в частности, к молекуле воды.

На результирующее значение дипольного момента молекулы может повлиять неподеленная пара электронов. Так, молекулы NH 3 и NF 3 имеют тетраэдрическую геометрию (с учетом неподеленной пары электронов). Степени ионности связей азот−водород и азот−фтор составляют 15 и 19%, соответственно, а их длины - 101 и 137 пм, соответственно. Исходя из этого, можно было бы сделать вывод о большем дипольном моменте NF 3 . Однако эксперимент показывает обратное. При более точном предсказании дипольного момента следует учитывать направление дипольного момента неподеленной пары (рис. 29).
Ковалентная, ионная и металлическая – три основных типа химических связей.
Познакомимся подробнее с ковалентной химической связью . Рассмотрим механизм ее возникновения. В качестве примера возьмем образование молекулы водорода:
Сферически симметричное облако, образованное 1s-электроном, окружает ядро свободного атома водорода. Когда атомы сближаются до определенного расстояния, происходит частичное перекрывание их орбиталей (см. рис.), в результате чего появляется молекулярное двухэлектронное облако между центрами обоих ядер, которое обладает максимальной электронной плотностью в пространстве между ядрами. При увеличении же плотности отрицательного заряда происходит сильное возрастание сил притяжения между молекулярным облаком и ядрами.
в результате чего появляется молекулярное двухэлектронное облако между центрами обоих ядер, которое обладает максимальной электронной плотностью в пространстве между ядрами. При увеличении же плотности отрицательного заряда происходит сильное возрастание сил притяжения между молекулярным облаком и ядрами.
Итак, мы видим, что ковалентная связь образуется путем перекрывания электронных облаков атомов, которое сопровождается выделением энергии. Если расстояние между ядрами у сблизившихся до касания атомов составляет 0,106 нм, тогда после перекрывания электронных облаков оно составит 0,074 нм. Чем больше перекрывание электронных орбиталей, тем прочнее химическая связь.
Ковалентной называется химическая связь, осуществляемая электронными парами . Соединения с ковалентной связью называют гомеополярными или атомными .
Существуют две разновидности ковалентной связи : полярная и неполярная .
При неполярной ковалентной связи образованное общей парой электронов электронное облако распределяется симметрично относительно ядер обоих атомов. В качестве примера могут выступать двухатомне молекулы, которые состоят из одного элемента: Cl 2 , N 2 , H 2 , F 2 , O 2 и другие, электронная пара в которых в принадлежит обоим атомам в одинаковой мере.
При полярной ковалентной связи электронное облако смещено к атому с большей относительной электроотрицательностью. Например молекулы летучих неорганических соединений таких как H 2 S, HCl, H 2 O и другие.
Образование молекулы HCl можно представить в следущем виде:
![]()
Т.к. относительная электроотрицательность атома хлора (2,83) больше, чем атома водорода (2,1), электронная пара смещается к атому хлора.
Помимо обменного механизма образования ковалентной связи – за счет перекрывания, также существует донорно-акцепторный механизм ее образования. Это механизм, при котором образование ковалентной связи происходит за счет двухэлектронного облака одного атома (донора) и свободной орбитали другого атома (акцептора). Давайте рассмотрим пример механизма образования аммония NH 4 + .В молекуле аммиака у атома азота есть двухэлектронное облако:
Ион водорода имеет свободную 1s-орбиталь, обозначим это как .
В процессе образования иона аммония двухэлектронное облако азота становится общим для атомов азота и водорода, это значит оно преобразуется в молекулярное электронное облако. Следовательно, появляется четвертая ковалентная связь. Можно представить процесс образования аммония такой схемой:
Заряд иона водорода рассредоточен между всеми атомами, а двухэлектронное облако, которое принадлежит азоту, становится общим с водородом.
Остались вопросы? Не знаете, как сделать домашнее задание?
Чтобы получить помощь репетитора – зарегистрируйтесь .
Первый урок – бесплатно!
сайт, при полном или частичном копировании материала ссылка на первоисточник обязательна.
Химическая связь.
Разные вещества имеют различное строение. Из всех известных на сегодняшний день веществ только инертные газы существуют в виде свободных (изолированных) атомов, что обусловлено высокой устойчивостью их электронных структур. Все другие вещества (а их в настоящее время известно более 10 млн.) состоят из связанных атомов.
Примечание: курсивом выделены те части текста, которые можно не учить и не разбирать.
Образование молекул из атомов приводит к выигрышу энергии, так как в обычных условиях молекулярное состояние устойчивее, чем атомное.
У атома на внешнем энергетическом уровне может содержаться от одного до восьми электронов. Если число электронов на внешнем уровне атома максимальное, которое он может вместить, то такой уровень называется завершенным . Завершенные уровни характеризуются большой прочностью. Таковы внешние уровни атомов благородных газов: у гелия на внешнем уровне два электрона (s 2), у остальных - по восемь электронов (ns 2 np 6). Внешние уровни атомов других элементов незавершенные и в процессе химического взаимодействия они завершаются.
Химическая связь образуется за счет валентных электронов, но осуществляется она по-разному. Различают три основных типа химических связей: ковалентную, ионную и металлическую.
Ковалентная связь
Механизм возникновения ковалентной связи рассмотрим на примере образования молекулы водорода:
Н + Н = Н 2 ; Q = 436 кДж
Ядро свободного атома водорода окружено сферически симметричным электронным облаком, образованным 1 s-электроном. При сближении атомов до определенного расстояния происходит частичное перекрывание их электронных облаков (орбиталей)
В результате между центрами обоих ядер возникает молекулярное двухэлектронное облако, обладающее максимальной электронной плотностью в пространстве между ядрами; увеличение же плотности отрицательного заряда благоприятствует сильному возрастанию сил притяжения между ядрами и молекулярным облаком.
Итак, ковалентная связь образуется в результате перекрывания электронных облаков атомов, сопровождающегося выделением энергии. Если у сблизившихся до касания атомов водорода расстояние между ядрами составляет 0,106 нм, то после перекрывания электронных облаков (образования молекулы Н 2) это расстояние составляет 0,074 нм. Наибольшее перекрывание электронных облаков осуществляется вдоль линии, соединяющей ядра двух атомов (это происходит при образовании σ–связи). Химическая связь тем прочнее, чем больше перекрывание электронных орбиталей. В результате возникновения химической связи между двумя атомами водорода каждый из них достигает электронной конфигурации атома благородного газа гелия.
Изображать химические связи принято по-разному:
1) с помощью электронов в виде точек, поставленных у химического знака элемента. Тогда образование молекулы водорода можно показать схемой
H∙ + H∙ →H:H
2) часто, особенно в органической химии, ковалентную связь изображают черточкой (штрихом) (например, Н-Н), которая символизирует общую пару электронов.
Ковалентная связь в молекуле хлора также осуществляется с помощью двух общих электронов, или электронной пары:
Неподеленная пара электронов, в атоме их 3
![]() ← Неподеленная пара электронов,
← Неподеленная пара электронов,
В молекуле их 6.
неспаренный электрон общая или поделенная пара электронов
Как видно, каждый атом хлора имеет три неподеленные пары и один неспаренный электрон. Образование химической связи происходит за счет неспаренных электронов каждого атома. Неспаренные электроны связываются в общую пару электронов, называемую также поделенной парой.
Если между атомами возникла одна ковалентная связь (одна общая электронная пара), то она называется одинарной; если больше, то кратной двойной (две общие электронные пары), тройной (три общие электронные пары).
Одинарная связь изображается одной черточкой (штрихом), двойная - двумя, тройная - тремя. Черточка между двумя атомами показывает, что у них пара электронов обобщена, в результате чего и образовалась химическая связь. С помощью таких черточек изображают структурные формулы молекул.
Итак, в молекуле хлора каждый его атом имеет завершенный внешний уровень из восьми электронов (s 2 p 6), причем два из них (электронная пара) в одинаковой мере принадлежат обоим атомам. Перекрывание электронных орбиталей при образовании молекулы показано на рис: 
В молекуле азота N 2 атомы имеют три общие электронные пары:
:N· + ·N: → :N:::N:
Очевидно, молекула азота прочнее молекулы водорода или хлора, чем и обусловлена значительная инертность азота в химических реакциях.
Химическая связь, осуществляемая электронными парами, называется ковалентной.
Механизмы образования ковалентной связи.
Ковалентная связь образуется не только за счет перекрывания одноэлектронных облаков, - это обменный механизм образования ковалентной связи.
При обменном механизме атомы предоставляют в общее пользование одинаковое количество электронов.
Возможен и другой механизм ее образования - донорно-акцепторный. В этом случае химическая связь возникает за счет неподеленной электронной пары одного атома и свободной орбитали другого атома.
Рассмотрим в качестве примера механизм образования иона аммония NH 4 +
При взаимодействии аммиака с НСl происходит химическая реакция:
NH 3 + HCl = NH 4 Cl или в сокращенном ионном виде: NH 3 + Н + = NH 4 +
При этом в молекуле аммиака атом азота имеет неподеленную пару электронов (двухэлектронное облако):
Ковалентная связь Механизм образования по Льюису.
Cвязь между атомами возникает при перекрывании их атомных орбиталей с образованием молекулярных орбиталей (МО). Различают два механизма образования ковалентной связи.
ОБМЕННЫЙ МЕХАНИЗМ - в образовании связи участвуют одноэлектронные атомные орбитали, т.е. каждый из атомов предоставляет в общее пользование по одному электрону:
ДOНОРНО-АКЦЕПТОРНЫЙ МЕХАНИЗМ - образование связи происходит за счет пары электронов атома-донора и вакантной орбитали атома-акцептора: \\
Характеристики ковалентной связи не зависят от механизма ее образования.
Свойства ковалентной связи: насыщаемость, направленность, гибридизация, кратность.
Особенностями ковалентной связи являются ее направленность и насыщаемость. Так как атомные орбитали пространственно ориентированы, то перекрывание электронных облаков происходит по определенным направлениям, что обусловливает направленность ковалентной связи. Количественно направленность выражается в виде валентных углов между направлениями химической связи в молекулах и твердых телах. Насыщаемость ковалентной связи вызывается ограничением числа электронов, находящихся на внешней оболочках, которые могут участвовать в образовании ковалентной связи.
Свойства КС:
1. Прочность КС – это свойства характер длинной связи (межъядерное пространство) и энергии энергией связи.
2. Полярность КС . В молекулах, содержащих ядра атомов одного и того же элемента, одна или несколько пар электронов в равной мере принадлежат обоим атомам, каждое ядро атома с одинаковой силой притягивает пару связывающих электронов. Такая связь называется неполярной ковалентной связью.
Если пара электронов, образующих химическую связь, смещена к одному из ядер атомов, то связь называют полярной ковалентной связью .
3. Насыщаемость КС – это способность атома участвовать только в определенном числе КС, насыщаемость характеризует валентностью атома. Количественные меры валентности явл. число не спаренных электронов у атома в основном и в возбужденном состоянии.
4. Направленность КС. Наиболее прочные КС образуются в направлении максимального перекрывания атомных орбиталей, т.е. мерой направленности служит валентный угол.
5. Гибридизация КС – при гибридизации происходит смещение атомных орбиталей, т.е. происходит выравнивание по энергии и по форме. Существует sp, sp 2 , sp 3 – гибридизация. sp – форма молекулы линейная (угол 180 0), sp 2 – форма молекулы плоская треугольная (угол 120 0), sp 3 - форма тетраэдрическая (угол 109 0 28).
6. Кратность КС или делоколизация связи – Число связей, образующихся между атомами, называется кратностью (порядком) связи. С увеличением кратности (порядка) связи изменяется длина связи и ее энергия.